题目内容
1.将纤维素水解得到的最终产物是C6H12O6,将之与NaClO3在酸性条件下反应生成ClO2.□C6H12O6+24NaClO3+12H2SO4=24ClO2↑+□CO2↑+18H2O+12Na2SO4下列叙述中正确的是( )| A. | 消耗0.8molNaClO3时,转移的电子数为0.8NA | |
| B. | H2O不是氧化产物,也不是还原产物,CO2是还原产物,ClO2是氧化产物 | |
| C. | 氧化剂和还原剂的物质的量之比为4:1 | |
| D. | 每生成1molCO2需转移24mol电子 |
分析 纤维素为多糖,水解最终产物葡萄糖具有还原性,可将NaClO3还原得到ClO2,Cl元素的化合价由+5价降低为+4价;葡萄糖中C元素的化合价升高,由于0升高为+4价,由电子守恒、原子守恒可知,反应为C6H12O6+24NaClO3+12H2SO4=24ClO2↑+6CO2↑+18H2O+12Na2SO4,结合氧化还原反应基本概念来解答.
解答 解:Cl元素的化合价由+5价降低为+4价,葡萄糖中C元素的化合价升高,由于0升高为+4价,由电子守恒、原子守恒可知,反应为C6H12O6+24NaClO3+12H2SO4=24ClO2↑+6CO2↑+18H2O+12Na2SO4,
A.NaClO3还原得到ClO2,Cl元素的化合价由+5价降低为+4价,则消耗0.8molNaClO3时,转移的电子数为0.8NA,故A正确;
B.CO2是氧化产物,ClO2是还原产物,故B错误;
C.氧化剂为NaClO3,还原剂为葡萄糖,则氧化剂和还原剂的物质的量之比为24:1,故C错误;
D.每生成1mol CO2需转移1mol×(4-0)=4mol电子,故D错误;
故选A.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,注意葡萄糖中C元素的化合价为0,侧重配平、基本概念及转移电子的考查,题目难度中等.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
11.设NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 1molH2O所含质子数为8NA | |
| B. | 1摩尔氦气所含的原子数为2NA | |
| C. | 在标准状况下1L水所含分子数为$\frac{1}{22.4}$NA | |
| D. | 0.5molaL与足量盐酸反应转移的电子数为1.5NA |
12.用NA表示阿伏加德罗常数的值.下列判断正确的是( )
| A. | 18 g H2O含有的氢原子数目为NA | |
| B. | 标准状况下,22.4LCO2含有的分子数目为NA | |
| C. | 1mol•L-1K2SO4溶液中含有的钾离子数目为2NA | |
| D. | 1mol H2在O2中完全燃烧转移的电子数目为NA |
9.下列有关物质检验的操作、现象及结论均正确的是( )
| 选项 | 实验操作及现象 | 实验结论 |
| A | 向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成 | 该溶液中一定含有SO42- |
| B | 向某溶液中加入稀盐酸,产生的气体通入澄清石灰水中,变石灰水浑浊 | 该溶液中一定含有CO32- |
| C | 向无色溶液中滴加氯水,再加CCl4振荡、静置、溶液分层,下层呈紫红色 | 该溶液中一定含有I- |
| D | 取洁净的铂丝在酒精灯火焰上灼烧至无色,再蘸取少量溶液置于火焰上灼烧,火焰呈黄色,通过蓝色钴玻璃观察,火焰呈紫色 | 该溶液一定含有Na+、K+ |
| A. | A | B. | B | C. | C | D. | D |
16.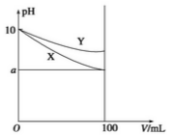 常温下,pH=10 的X、Y 两种碱溶液各1mL,分别稀释到100mL,其pH 与溶液体积(V)的关系如图所示,下列说法正确的是( )
常温下,pH=10 的X、Y 两种碱溶液各1mL,分别稀释到100mL,其pH 与溶液体积(V)的关系如图所示,下列说法正确的是( )
 常温下,pH=10 的X、Y 两种碱溶液各1mL,分别稀释到100mL,其pH 与溶液体积(V)的关系如图所示,下列说法正确的是( )
常温下,pH=10 的X、Y 两种碱溶液各1mL,分别稀释到100mL,其pH 与溶液体积(V)的关系如图所示,下列说法正确的是( )| A. | 若8<a<10,则X、Y 都是弱碱 | |
| B. | 稀释后,X 溶液的碱性比Y 溶液的碱性强 | |
| C. | X、Y 两种碱溶液中溶质的物质的量浓度一定相等 | |
| D. | 分别完全中和X、Y 这两种碱溶液时,消耗同浓度盐酸的体积VX>VY |
6.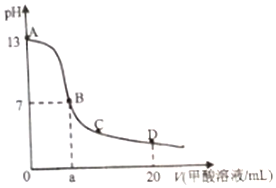 在15mL0.lmol•L-1KOH溶液中逐滴加入0.2mol•L-1甲酸溶液,溶液pH和加入甲酸(弱酸)的体积关系曲线如图所示,下列关系正确的是( )
在15mL0.lmol•L-1KOH溶液中逐滴加入0.2mol•L-1甲酸溶液,溶液pH和加入甲酸(弱酸)的体积关系曲线如图所示,下列关系正确的是( )
 在15mL0.lmol•L-1KOH溶液中逐滴加入0.2mol•L-1甲酸溶液,溶液pH和加入甲酸(弱酸)的体积关系曲线如图所示,下列关系正确的是( )
在15mL0.lmol•L-1KOH溶液中逐滴加入0.2mol•L-1甲酸溶液,溶液pH和加入甲酸(弱酸)的体积关系曲线如图所示,下列关系正确的是( )| A. | 在B点:c(K+)=c(HCOO-)>c(OH-)=c(H+),且a=7.5 | |
| B. | 在A、B间任意一点,c(HCOO-)>c(K+)>c(OH-)>c(H+) | |
| C. | 在D点:c(HCOO-)+c(HCOOH)>2c(K+) | |
| D. | B→C段:水的电离程度先增大后减小 |
13.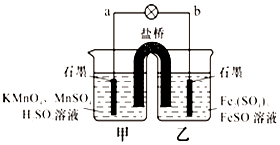 某合作学习小组的同学利用下列氧化还原反应设计原电池:2KMnO4+10FeSO4+8H2SO4═2MnSO4+5Fe2(SO4)3+K2SO4+8H2O盐桥中装有饱和K2SO4溶液,下列叙述中正确的是( )
某合作学习小组的同学利用下列氧化还原反应设计原电池:2KMnO4+10FeSO4+8H2SO4═2MnSO4+5Fe2(SO4)3+K2SO4+8H2O盐桥中装有饱和K2SO4溶液,下列叙述中正确的是( )
 某合作学习小组的同学利用下列氧化还原反应设计原电池:2KMnO4+10FeSO4+8H2SO4═2MnSO4+5Fe2(SO4)3+K2SO4+8H2O盐桥中装有饱和K2SO4溶液,下列叙述中正确的是( )
某合作学习小组的同学利用下列氧化还原反应设计原电池:2KMnO4+10FeSO4+8H2SO4═2MnSO4+5Fe2(SO4)3+K2SO4+8H2O盐桥中装有饱和K2SO4溶液,下列叙述中正确的是( )| A. | 外电路的电流方向是从a到b | |
| B. | 甲烧杯中溶液的pH逐渐减小 | |
| C. | 电池工作时,盐桥中的SO42-移向甲烧杯 | |
| D. | 乙烧杯中发生还原反应 |
10.CO2的摩尔质量为( )
| A. | 44g | B. | 44g/mol | C. | 44 | D. | 22.4L/mol |
10.等物质的量的下列化合物与足量浓盐酸反应,得到氯气的物质的量最多的是( )
| A. | KClO3 | B. | KMnO4 | C. | MnO2 | D. | Ca(ClO)2 |