题目内容
【题目】如图所示,用石墨电极电解饱和食盐水。下列说法不正确的是( )
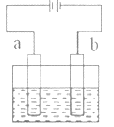
A.通电使NaCl 发生电离
B.电极a 是阳极
C.Na+向 b 极移动
D.a 极产生黄绿色气体
【答案】A
【解析】
与电源的正极相连的是阳极,与电源的负极相连的是阴极,所以a极是阳极,b极是阴极;阳离子向阴极移动,阴离子向阳极移动;电解饱和食盐水,阳极电极反应式为:2Cl--2e-=Cl2↑,阴极电极反应式为:2H++2e-=H2↑。
A.NaCl在水中就能发生电离,通电不是必要条件,A错误;
B.电极a与电源的正极相连,是阳极,B正确;
C.阳离子向阴极移动,b极是阴极,Na+向b极移动,C正确;
D. a极为阳极,其电极反应式为:2Cl--2e-=Cl2↑,产生黄绿色气体,D正确;故答案为:A。

 名校课堂系列答案
名校课堂系列答案【题目】![]() 时,向容积为2L的恒容密闭容器中充入一定量的CO和
时,向容积为2L的恒容密闭容器中充入一定量的CO和![]() ,发生如下反应:
,发生如下反应:![]() 。反应过程中测定的部分数据见下表:
。反应过程中测定的部分数据见下表:
反应时间 |
|
|
0 |
|
|
20 |
|
|
30 |
|
|
下列说法正确的是
A.反应在![]() 内的平均速率为
内的平均速率为![]()
B.保持其他条件不变,升高温度,平衡时![]() ,则反应的
,则反应的![]()
C.保持其他条件不变,再向平衡体系中同时通入![]() 、
、![]() 、
、![]() ,达到新平衡前
,达到新平衡前![]() 正
正![]() 逆
逆![]()
D.相同温度下,若起始时向容器中充入![]() ,达到平衡时
,达到平衡时![]() 转化率大于
转化率大于![]()
【题目】I.NaHSO3、CuSO4为实验室常用的化学试剂,均易溶于水,且水溶液显酸性。在铁片镀铜实验中,为提高电镀效果,常用CuSO4溶液作为电镀液。装置如图所示,a接电源_____极,阳极的电极反应式为:_____。电镀过程中c(Cu2+)_____(填“基本不变”、“变大”或“变小”)。

II.某实验小组对NaHSO3溶液分别与CuSO4、CuCl2溶液的反应进行探究。
实验 | 装置 | 试剂x | 操作及现象 |
A |
| 1mol·L1CuSO4溶液 | 加入2mLCuSO4溶液,得到绿色溶液,3分钟未见明显变化。 |
B | 1mol·L1CuCl2溶液 | 加入2mLCuCl2溶液,得到绿色溶液,30s时有无色气泡和白色沉淀产生,上层溶液颜色变浅。 |
(1)推测实验B产生的无色气体为SO2,实验证实推测正确:用蘸有碘水的淀粉试纸接近试管口,观察到_____,反应的离子方程式为_____。
(2)对实验B产生SO2的原因进行分析,提出假设:
假设a:Cu2+水解使溶液中c(H+)增大;
假设b:Cl-存在时,Cu2+与HSO![]() 反应生成CuCl白色沉淀,溶液中c(H+)增大。
反应生成CuCl白色沉淀,溶液中c(H+)增大。
①假设a不合理,实验证据是_____;
②实验表明假设b合理,实验B反应的离子方程式有_____、H++HSO![]() =SO2↑+H2O。
=SO2↑+H2O。
(3)对比实验A、B,提出假设:Cl-增强了Cu2+的氧化性。下述实验C证实了假设合理,装置如图(两个电极均为碳棒)。实验方案:闭合K,电压表的指针偏转至“X”处;向U形管_____________________________________(补全实验操作及现象)。

(4)将实验A的溶液静置24小时或加热后,得到红色沉淀。经检验,红色沉淀中含有Cu+、Cu2+和SO![]() 。已知:
。已知:
I.![]() ;
;
II.
III.Cu2O是一种红色粉末状固体,几乎不溶于水,但溶于氨水,成稳定的、无色的配合物[Cu(NH3)2]+。
①通过实验D证实红色沉淀中含有Cu+和Cu2+。
实验D:
证实红色沉淀中含有Cu+的实验证据是_____;
②有同学认为实验D不足以证实红色沉淀中含有Cu2+,设计实验D的对比实验E,证实了Cu2+的存在。实验E的方案和现象是_____。(要求:用图示表示,参照实验D)
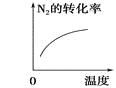
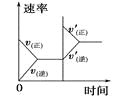
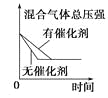
【题目】对于可逆反应N2(g)+3H2(g) ![]() 2NH3(g) △H<0,下列研究目的和示意图相符的是( )
2NH3(g) △H<0,下列研究目的和示意图相符的是( )
A | B | C | D | |
研究目的 | 压强对反应的影响 (p2>p1) | 温度对反应的影响 | 平衡体系中增加N2的浓度对反应的影响 | 催化剂对反应的影响 |
示意图 |
|
|
|
|
A.AB.BC.CD.D