题目内容
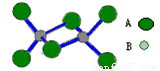
如图是某无机化合物的二聚分子,该分子中A、B两种元素都是第3周期的元素,分子中所有原子的最外层都达到了8个电子的稳定结构.下列说法不正确的是( )
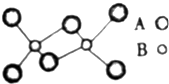
| A.B原子很可能采取sp3杂化 |
| B.该化合物的化学式是Al2Cl6 |
| C.该化合物是离子化合物,在熔融状态下能导电 |
| D.该化合物中不存在离子键,也不存在非极性共价键 |

A、因B原子与相连的四个原子形成四面体,则中心原子采取sp3杂化,故A正确;
B、将二聚分子变成单分子,得AB3化学式,根据两种元素都处于第三周期,可能是PCl3 或AlCl3,而在PCl3所有原子已达稳定结构,形成二聚分子的话不可能符合,故只可能是AlCl3,该化合物的化学式是Al2Cl6,故B正确;
C、该化合物是无机化合物的二聚分子,属于共价化合物,不存在离子键,也不是离子化合物,故C错误;
D、该化合物是无机化合物的二聚分子,属于共价化合物,不存在离子键;Cl与Cl之间没有形成非极性共价键,故D正确;
故选C.
B、将二聚分子变成单分子,得AB3化学式,根据两种元素都处于第三周期,可能是PCl3 或AlCl3,而在PCl3所有原子已达稳定结构,形成二聚分子的话不可能符合,故只可能是AlCl3,该化合物的化学式是Al2Cl6,故B正确;
C、该化合物是无机化合物的二聚分子,属于共价化合物,不存在离子键,也不是离子化合物,故C错误;
D、该化合物是无机化合物的二聚分子,属于共价化合物,不存在离子键;Cl与Cl之间没有形成非极性共价键,故D正确;
故选C.

练习册系列答案
相关题目
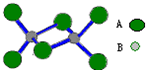 (2011?上海模拟)如图是某无机化合物的二聚分子,该分子中A、B两种元素都是第三周期的元素,分子中所有原子的最外层电子都达到8个电子的稳定结构.下列说法不正确的是( )
(2011?上海模拟)如图是某无机化合物的二聚分子,该分子中A、B两种元素都是第三周期的元素,分子中所有原子的最外层电子都达到8个电子的稳定结构.下列说法不正确的是( )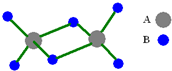 如图是某无机化合物的二聚分子,该分子中A、B两种元素都是第三周期的元素,分子中所有原子的最外层电子都达到8个电子的稳定结构.下列说法不正确的是( )
如图是某无机化合物的二聚分子,该分子中A、B两种元素都是第三周期的元素,分子中所有原子的最外层电子都达到8个电子的稳定结构.下列说法不正确的是( )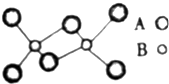 如图是某无机化合物的二聚分子,该分子中A、B两种元素都是第3周期的元素,分子中所有原子的最外层都达到了8个电子的稳定结构.下列说法不正确的是( )
如图是某无机化合物的二聚分子,该分子中A、B两种元素都是第3周期的元素,分子中所有原子的最外层都达到了8个电子的稳定结构.下列说法不正确的是( ) A.该化合物的化学式是Al2Cl6
A.该化合物的化学式是Al2Cl6