题目内容
某学生用标准的已知浓度的稀盐酸来滴定一未知浓度的NaOH溶液,下列操作可能会使溶液浓度的测定值偏低的是( )
| A、滴定管出口部分开始有气泡,滴定后气泡消失 |
| B、锥形瓶用蒸馏水冲洗后随即使用 |
| C、当看到锥形瓶中溶液的颜色发生变化后随即停止了滴定 |
| D、滴定管在用蒸馏水洗净后,即装入标准的酸溶液进行滴定 |
考点:中和滴定
专题:化学实验基本操作
分析:根据c(待测)=
分析不当操作对V(标准)的影响,V(标准)偏大,c(待测)偏大,V(标准)偏小,c(待测)偏小,以此判断浓度的误差.
| c(标准)×V(标准) |
| V(待测) |
解答:
解:A.酸式滴定管在滴定前有气泡,滴定后气泡消失,造成V(标准)偏大,根据c(待测)=
,可知c(待测)偏大,故A错误;
B.锥形瓶用蒸馏水洗净后未烘干,待测液的物质的量不变,V(标准)不变,所以c(待测)不变,故B错误;
C.指示剂局部的颜色有变化就停止滴定,反应还没有结束,导致消耗的标准液体积偏小,测定结果偏低,故C正确;
D.酸式滴定管未润洗就装标准液滴定,标准液被稀释,浓度偏小,造成V(标准)偏大,根据c(待测)=
,可知c(待测)偏大,故D错误;
故选:C.
| c(标准)×V(标准) |
| V(待测) |
B.锥形瓶用蒸馏水洗净后未烘干,待测液的物质的量不变,V(标准)不变,所以c(待测)不变,故B错误;
C.指示剂局部的颜色有变化就停止滴定,反应还没有结束,导致消耗的标准液体积偏小,测定结果偏低,故C正确;
D.酸式滴定管未润洗就装标准液滴定,标准液被稀释,浓度偏小,造成V(标准)偏大,根据c(待测)=
| c(标准)×V(标准) |
| V(待测) |
故选:C.
点评:本题主要考查了中和滴定操作的误差分析,根据c(待测)=
,是解答的关键,题目难度不大.
| c(标准)×V(标准) |
| V(待测) |

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
能正确表示下列反应的离子方程式的是( )
| A、硫化亚铁溶于稀硝酸中:FeS+2H+=Fe2++H2S↑ |
| B、用FeCl3溶液腐蚀印刷电路板:Fe3++Cu=Fe2++Cu2+ |
| C、向明矾溶液中加入过量氢氧化钡溶液:Al3++2SO2-4+2Ba2++4OH-=2BaSO4↓+AlO-2+2H2O |
| D、等物质的量的NaHCO3和Ca(OH)2溶液混合:2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O |
下列叙述不正确的是( )
| A、在实验室里硅酸钠溶液存放在带橡胶塞的试剂瓶中 |
| B、提倡人们购物时不用塑料袋,是为了防止白色污染 |
| C、氟利昂(CCl2F2)因破坏大气臭氧层而导致“温室效应” |
| D、为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术 |
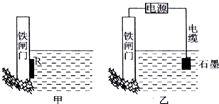
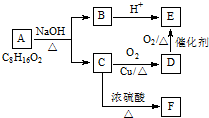
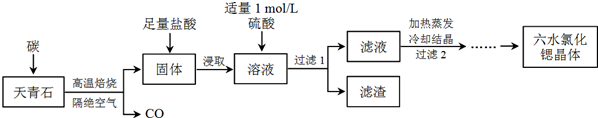
 化学反应原理在生活和生产中有着广泛的应用.利用“化学蒸气转移法”制备TaS2晶
化学反应原理在生活和生产中有着广泛的应用.利用“化学蒸气转移法”制备TaS2晶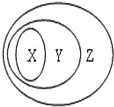 用如图表示的一些物质或概念间的从属关系中不正确的是( )
用如图表示的一些物质或概念间的从属关系中不正确的是( )