题目内容
14.下列物质中:①NaCl溶液 ②氢氧化钠 ③二氧化碳 ④金刚石 ⑤水 ⑥酒精,属于电解质的是②⑤;非电解质的是③⑥.(请用序号填空)分析 在水溶液里或熔融状态下能导电的化合物是电解质;
在水溶液里和熔融状态下都不导电的化合物是非电解质.
解答 解:①NaCl溶液是混合物,属于电解质溶液,
②氢氧化钠水溶液中导电属于电解质,
③二氧化碳不能发生电离,属于非电解质,
④金刚石是单质,既不是电解质也不是非电解质,
⑤水存在微弱电离属于弱电解质,
⑥酒精本身不能电离属于非电解质,
属于电解质的是②⑤,非电解质的是③⑥,
故答案为:②⑤; ③⑥;
点评 本题考查了电解质和非电解质基本概念,知道概念的内涵即可解答,注意二氧化碳的水溶液能导电,但二氧化碳为非电解质,题目难度不大.

练习册系列答案
 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
8.在指定环境中,下列各组离子可以大量共存的是( )
| A. | 加入铝片立即放出氢气的溶液中:C1-、K+、NH4+、NO3- | |
| B. | 滴加石蕊试液呈红色的溶液中:CO32-、K+、ClO-、OH- | |
| C. | pH=13的溶液中:HCO3-、Na+、NO3-、SO42 | |
| D. | 在pH=3的溶液中:NH4+、Ca2+、C1-、K+ |
9.将29.5g乙烷与乙烯的混合气体通入足量溴水,可使溴水增重7g,据此可推知混合气体中乙烯所占体积分数为( )
| A. | 20% | B. | 23.7% | C. | 25% | D. | 无法确定 |
19.氢键既可以存在于分子之间,也可以存在于分子内部的原子团之间,如邻羟基苯甲酸(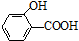 )存在分子内氢键,对羟基苯甲酸 (
)存在分子内氢键,对羟基苯甲酸 ( 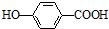 )存在分子间氢键.则两者的熔点、沸点的相对大小关系是( )
)存在分子间氢键.则两者的熔点、沸点的相对大小关系是( )
 )存在分子内氢键,对羟基苯甲酸 (
)存在分子内氢键,对羟基苯甲酸 (  )存在分子间氢键.则两者的熔点、沸点的相对大小关系是( )
)存在分子间氢键.则两者的熔点、沸点的相对大小关系是( )| A. | 前者>后者 | B. | 前者<后者 | C. | 前者=后者 | D. | 无法估计 |
3.下列粒子结构示意图中,表示Mg2+的是( )
| A. | 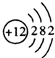 | B. | 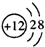 | C. | 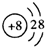 | D. | 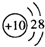 |
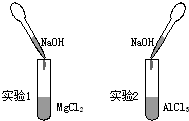 (1)已知反应:H2+Cl2$→_{400℃}^{CuO/CuCl_{2}}$2HCl,已知H-H键能为436kJ/mol,Cl-Cl键能为243kJ/mol,H-Cl键能为432kJ/mol.
(1)已知反应:H2+Cl2$→_{400℃}^{CuO/CuCl_{2}}$2HCl,已知H-H键能为436kJ/mol,Cl-Cl键能为243kJ/mol,H-Cl键能为432kJ/mol. ;
; +3HNO3$→_{△}^{浓硫酸}$
+3HNO3$→_{△}^{浓硫酸}$ +3H2O;
+3H2O; 的系统命名是:2,6-二甲基辛烷;
的系统命名是:2,6-二甲基辛烷; 的键线式是
的键线式是 ;
; 的分子中含有3个手性碳原子;
的分子中含有3个手性碳原子; .
.