题目内容
12.下列说法正确的是(NA表示阿伏加德罗常数的值)( )| A. | 11.2 L N2含有的分子数为0.5NA | |
| B. | 在常温常压下,1 mol Ne含有的原子数为NA | |
| C. | 71 g Cl2所含分子数为2NA | |
| D. | 在同温同压下,相同体积的任何气体单质所含的原子数相同 |
分析 A、氮气所处的状态不明确;
B、氖为单原子分子;
C、氯气的分子个数N=$\frac{m}{M}{N}_{A}$来计算;
D、气体单质分为单原子分子、双原子分子和多原子分子.
解答 解:A、氮气所处的状态不明确,故氮气的物质的量无法计算,故A错误;
B、氖为单原子分子,则1mol氖气中含1mol氖原子即NA个,故B正确;
C、71g氯气中的分子个数N=$\frac{m}{M}{N}_{A}$=$\frac{71g}{71g/mol}$NA=NA个,故C错误;
D、同温同压下,相同体积的气体单质的物质的量相同,但由于气体单质分为单原子分子、双原子分子和多原子分子,故所含的原子个数不一定相同,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
2.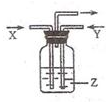 下列各组物质中.气体X和气体Y在通常条件下同时通入盛有溶液z的洗气瓶中(如图所示),一定没有沉淀生成的是( )
下列各组物质中.气体X和气体Y在通常条件下同时通入盛有溶液z的洗气瓶中(如图所示),一定没有沉淀生成的是( )
 下列各组物质中.气体X和气体Y在通常条件下同时通入盛有溶液z的洗气瓶中(如图所示),一定没有沉淀生成的是( )
下列各组物质中.气体X和气体Y在通常条件下同时通入盛有溶液z的洗气瓶中(如图所示),一定没有沉淀生成的是( )| X | Y | Z | |
| A | NO2 | SO2 | BaCl2 |
| B | NH3 | O2 | Al2(SO4)3 |
| C | NH3 | CO2 | NaCl(饱和) |
| D | CO | O2 | Ca(OH)2 |
| A. | A | B. | B | C. | C | D. | D |
3.下列各组元素性质递变情况错误的是( )
①Li、B、Be原子最外层电子数依次增多
②P、S、Cl元素最高正化合价依次升高
③B、C、N、O、F原子半径依次增大
④Li、Na、K、Rb的原子半径依次增大.
①Li、B、Be原子最外层电子数依次增多
②P、S、Cl元素最高正化合价依次升高
③B、C、N、O、F原子半径依次增大
④Li、Na、K、Rb的原子半径依次增大.
| A. | ① | B. | ①③ | C. | ③ | D. | ②④ |
7.按照物质的树状分类和交叉分类,HNO3应属于( )
①酸 ②氢化物 ③氧化物 ④含氧酸 ⑤难挥发性 ⑥强氧化性 ⑦一元酸 ⑧化合物 ⑨混合物.
①酸 ②氢化物 ③氧化物 ④含氧酸 ⑤难挥发性 ⑥强氧化性 ⑦一元酸 ⑧化合物 ⑨混合物.
| A. | ①②③④⑤⑥⑦⑧ | B. | ①④⑥⑦⑧ | C. | ①⑨ | D. | ①④⑤⑥⑦ |
17.在5KCl+KClO3+3H2SO4=3Cl2↑+3K2SO4+3H2O中,被氧化的氯元素与被还原的氯元素的质量比为( )
| A. | 1:1 | B. | 5:1 | C. | 1:5 | D. | 3:1 |
1.有关金属钠的叙述正确的是 ( )
| A. | 钠的密度比煤油大,保存在煤油中 | |
| B. | 金属钠质软,可以用小刀切割 | |
| C. | 钠的熔点比水大,钠投入到水中放热反应生成的气体中有大量水蒸气 | |
| D. | Na比Cu活泼,因而可以从Cu的盐溶液中置换出铜 |

 某校研究性学习小组的同学对金属镁在空气中燃烧的产物进行探究.
某校研究性学习小组的同学对金属镁在空气中燃烧的产物进行探究.