题目内容
将0.4克NaCl和KI的混合物溶于水,再向此溶液中加入过量的AgNO3溶液,析出沉淀的质量为0.898克,求NaCl和KI混合物中各组分的百分含量为多少?
答案:
解析:
解析:
|
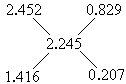
解: mAgCl/NaCl= m沉淀/原混合物= 应用十字交叉法: ∴KI%= 分析: NaCl、KI与AgNO3反应的方程式是: NaCl+AgNO3 KI+AgNO3=AgI↓+KNO3 58.5g NaCl生成143.3g AgCl沉淀,166g KI生成234.8克AgI沉淀.现在混合物为NaCl、KI,则生成沉淀量在这两沉淀之间.混合物的沉淀又为AgCl、AgI两沉淀之和,故符合使用十字交叉法条件. |

练习册系列答案
相关题目
下面是四种盐在不同温度下的溶解度(克/100克水)
| NaNO3 | KNO3 | NaCl | KCl | |
| 10℃ | 80.5 | 20.9 | 35.7 | 31.0 |
| 100℃ | 175 | 246 | 39.1 | 56.6 |
(计算时假定:①盐类共存时不影响各自的溶解度;②过滤晶体时,溶剂损耗忽略不计。)
(1)取23.4克NaCl和40.4克KNO3,加70.0克H2O,加热溶解。在100℃时蒸发掉50.0克H2O,维 持该温度,过滤出晶体,计算所得晶体的质量(m高温)。将滤液冷却至10℃,待充分结晶后,过滤。计算所得晶体的质量(m低温)。
(2)另取34.0克NaNO3和29.8克KCl,同样进行如上实验。10℃时析出的晶体是 (写化学式)。100℃和10℃得到的晶体质量(m高温和m低温)分别是多少?