题目内容
质量分数为a的KOH溶液mg与质量分数为b的该溶液mg混合后,得到KOH物质的量浓度为c mol/L的混合溶液.则所得混合溶液的密度为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
考点:物质的量浓度的相关计算
专题:物质的量浓度和溶解度专题
分析:根据m(溶质)=m(溶液)w(溶质)计算KOH的质量,根据n=
计算KOH的物质的量,再根据V=
计算溶液的体积,根据ρ=
计算溶液的密度.
| m |
| M |
| n |
| c |
| m |
| V |
解答:
解:混合后KOH的质量=m(a+b)g,
则KOH的物质的量=
=
mol,
溶液体积=
=
L,
故溶液的密度=
=
g/cm3
故选A.
则KOH的物质的量=
| m(a+b)g |
| 56g/mol |
| m(a+b) |
| 56 |
溶液体积=
| ||
| c mol/L |
| m(a+b) |
| 56c |
故溶液的密度=
| 2m g | ||
|
| 112c |
| 1000(a+b) |
故选A.
点评:本题考查物质的量浓度、质量分数有关计算,属于字母型计算,增大题目难度,注意对公式的理解与灵活应用.

练习册系列答案
相关题目
为“绿色奥运”某同学提出了下列环保建议,其中你认为可以采纳的是( )
①用气态燃料代替液态和固态燃料作为发动机动力来源;②开发生产无汞电池;③提倡使用一次性塑料餐具和塑料袋,以防传染疾病;④分类回收垃圾;⑤开发无磷洗涤剂;⑥提倡使用手帕,减少餐巾纸的使用.
①用气态燃料代替液态和固态燃料作为发动机动力来源;②开发生产无汞电池;③提倡使用一次性塑料餐具和塑料袋,以防传染疾病;④分类回收垃圾;⑤开发无磷洗涤剂;⑥提倡使用手帕,减少餐巾纸的使用.
| A、①③③④ | B、②③④⑤ |
| C、①②④⑤⑥ | D、全部 |
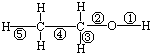 乙醇分子中不同的化学键如图.下列关于乙醇在不同的反应中断裂化学键的说法错误的是( )
乙醇分子中不同的化学键如图.下列关于乙醇在不同的反应中断裂化学键的说法错误的是( )| A、与金属钠反应时,键①断裂 |
| B、在Ag催化下与O2反应时,键①、③断裂 |
| C、与CuO反应时,键①断裂 |
| D、与浓硫酸共热至140℃时,键①或键②断裂;共热至170℃时,键②、⑤断裂 |
常温下,下列各组离子在指定溶液中可能大量共存的是( )
| A、在碱性溶液中:K+、Cl-、Na+、CO32- | ||||
B、在
| ||||
| C、澄清透明溶液中:Cu2+、Fe3+、I-、SO42- | ||||
D、与铝粉反应放出氢气的无色溶液中:K+、N
|
把5molA和6molB的混合气体通入4L的密闭容器中,在一定条件下发生如下反应:5A(g)+4B(g)?6C(g)+xD(g),经过5min后反应达到平衡状态时,生成3mol C,并测得D的平均反应速率为0.1mol?L-1?min-1.下列计算结果正确的是( )
| A、x的数值是2 |
| B、A的转化率为40% |
| C、B的平衡浓度为4mol/L |
| D、反应前后混合气体的压强之比为22:23 |
下列物质中,导电性能最差的是( )
| A、石墨棒 | B、盐酸溶液 |
| C、熔融氢氧化钠 | D、固体氯化钾 |
下列反应中,属于加成反应的是( )
| A、2Na+2C2H5OH→2C2H5ONa+H2↑ | |||
B、CH2=CH2+HCl
| |||
C、2CH3CHO+O2
| |||
D、 +Br2 +Br2
 +HBr +HBr |
下列说法正确的是( )
| A、海水中含量最高的元素是氯 |
| B、海水中含量最高的物质是氯化钠 |
| C、加碘食盐溶液遇淀粉溶液显蓝色 |
| D、加碘食盐中的碘是含碘元素的化合物 |
下燃烧0.1mol两种气态烃的混合物,生成3.58L CO2(标准状况)和3.60g H2O,则混合气体中( )
| A、一定有甲烷 |
| B、一定有乙烷 |
| C、一定无甲烷 |
| D、一定有丙烷 |