题目内容
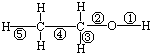 乙醇分子中不同的化学键如图.下列关于乙醇在不同的反应中断裂化学键的说法错误的是( )
乙醇分子中不同的化学键如图.下列关于乙醇在不同的反应中断裂化学键的说法错误的是( )| A、与金属钠反应时,键①断裂 |
| B、在Ag催化下与O2反应时,键①、③断裂 |
| C、与CuO反应时,键①断裂 |
| D、与浓硫酸共热至140℃时,键①或键②断裂;共热至170℃时,键②、⑤断裂 |
考点:有机物的结构和性质
专题:有机反应
分析:A.与Na反应生成氢气,O-H键断裂;
B.在Ag催化下与O2反应时,生成醛,C-H、O-H键断裂;
C.与CuO发生氧化反应生成醛,C-H、O-H键断裂;
D.与浓硫酸共热至140℃时,生成乙醚,C-O或O-H键断裂;共热至170℃时生成乙烯,C-O和C-H键断裂.
B.在Ag催化下与O2反应时,生成醛,C-H、O-H键断裂;
C.与CuO发生氧化反应生成醛,C-H、O-H键断裂;
D.与浓硫酸共热至140℃时,生成乙醚,C-O或O-H键断裂;共热至170℃时生成乙烯,C-O和C-H键断裂.
解答:
解:A.与Na反应生成氢气,O-H键断裂,即①断裂,故A正确;
B.在Ag催化下与O2反应时,生成醛,C-H、O-H键断裂,则键①、③断裂,故B正确;
C.与CuO发生氧化反应生成醛,C-H、O-H键断裂,则键①、③断裂,故C错误;
D.与浓硫酸共热至140℃时,生成乙醚,C-O或O-H键断裂,即键①或②断裂;共热至170℃时生成乙烯,C-O和C-H键断裂,键②、⑤键断裂,故D正确.
故选C.
B.在Ag催化下与O2反应时,生成醛,C-H、O-H键断裂,则键①、③断裂,故B正确;
C.与CuO发生氧化反应生成醛,C-H、O-H键断裂,则键①、③断裂,故C错误;
D.与浓硫酸共热至140℃时,生成乙醚,C-O或O-H键断裂,即键①或②断裂;共热至170℃时生成乙烯,C-O和C-H键断裂,键②、⑤键断裂,故D正确.
故选C.
点评:本题考查有机物的结构与性质,侧重乙醇性质的考查,注意乙醇的性质与官能团、化学键的关系,注重基础知识的考查,题目难度不大.

练习册系列答案
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案
相关题目
下列有关中和热测定实验说法正确的是( )
| A、中和热测定实验中可以用环形铁丝搅拌棒比环形玻璃搅拌棒更方便 |
| B、中和热测定实验中若将50mL 0.50mol/L盐酸和50mL 0.55mol/L NaOH溶液改为100mL 0.50mol/L盐酸和100mL 0.55mol/L NaOH溶液,所测中和热数值将变为原实验的2倍 |
| C、教材中和热测定实验中所取NaOH的物质的量稍大于HCl,会导致所测中和热数值偏高 |
| D、做1次完整的中和热测定实验,温度计需使用3次 |
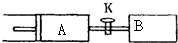 如图所示,向A、B中均充入1mol X、lmol Y,起始时A、B的体积都等于a L.在相同温度、外界压强和催化剂存在的条件下,关闭活塞K,使两容器中都发生下述反应:X(g)+Y(g)═2Z(g)+W(g)△H<0.达平衡时,A的体积为1.4a L.下列说法错误的是( )
如图所示,向A、B中均充入1mol X、lmol Y,起始时A、B的体积都等于a L.在相同温度、外界压强和催化剂存在的条件下,关闭活塞K,使两容器中都发生下述反应:X(g)+Y(g)═2Z(g)+W(g)△H<0.达平衡时,A的体积为1.4a L.下列说法错误的是( )| A、反应速率:v(B)>v(A) |
| B、A容器中X的转化率为80% |
| C、平衡时的压强:PB=PA |
| D、平衡时Y体积分数:A<B |
下列与阿伏加德罗常数的值(NA)有关的说法正确的是( )
| A、NA个Fe(OH)3胶体粒子的质量为107g |
| B、3mol NF3与水完全反应生成HNO3和NO,转移电子数2NA |
| C、标准状况下,2.24L Cl2溶于水中达到饱和,可得到HClO分子的数目是0.1NA |
| D、常温常压下,1.7g H2O2中含有的电子数为NA |
水溶液的pH值最大( )
| A、NaHCO3 |
| B、KHSO4 |
| C、AlCl3 |
| D、HF |
可用Zn+Br2═ZnBr2 设计成蓄电池,其中负极反应是( )
| A、Zn→Zn2++2e- |
| B、Br2+2e-→2Br- |
| C、2Br→Br2+2e- |
| D、Zn2++2e-→Zn |
下列现象或事实可用同一原理解释的是( )
| A、浓硫酸和浓盐酸长期暴露在空气中浓度均降低 |
| B、氯水和双氧水均要盛装在棕色试剂瓶中 |
| C、SO2能使品红溶液和溴水均褪色 |
| D、NaCl固体中混有NH4Cl或I2,均可用加热法除去 |
质量分数为a的KOH溶液mg与质量分数为b的该溶液mg混合后,得到KOH物质的量浓度为c mol/L的混合溶液.则所得混合溶液的密度为( )
A、
| ||
B、
| ||
C、
| ||
D、
|