��Ŀ����
Q��W��X��Y��Z��ԭ��������������Ķ�����Ԫ�أ�X��Y�ǽ���Ԫ�أ�X��ɫ��ɫ������Ԫ�غ˵����֮��Ϊ54������������֮��Ϊ20��W��Z������������ͬZ�ĺ˵������W��2������ҵ��һ��ͨ�������������Y���ʡ�������˵������ȷ��( )
A��X��Y������������Ӧ��ˮ����֮��ɷ�����Ӧ
B��Q��W���γ�ԭ�Ӹ�����Ϊ1:1��1:2�ij���������
C��Y��Z���γɵĻ�������ˮ��Ӧ�����������г�������
D��X��W֮����γ��������Ӹ�����Ϊ1:1��1:2�ij���������
D
��������
���������X��ɫ��ɫ��X��Na��Q��W��X��Y��Z��ԭ��������������Ķ�����Ԫ�أ�W��Z������������ͬZ�ĺ˵������W��2������W��O;Z��S��X��Y�ǽ���Ԫ�أ���ҵ��һ��ͨ�������������Y���ʡ���Y��Al������Ԫ�غ˵����֮��Ϊ54������������֮��Ϊ20����Q��C����������Ԫ�طֱ��ǣ�C O Na Al S��A��NaOH��ǿ�Al(OH)3����������������߿ɷ�����Ӧ����ƫ�����ƺ�ˮ����ȷ��BQ��W���γ�CO ��CO2����ȷ��C��Al2S3�����������Σ���ˮ�з���˫ˮ�ⷴӦ�������������������������塣��ȷ��D��X��W֮����γ�Na2O ��Na2O2���ֳ�����������ǵ��������Ӹ����ȶ���Ϊ2:1������
���㣺����Ԫ�����ڱ���Ԫ�������ɵ�֪ʶ��

| A���⻯���ȶ��ԣ�Z��W | B��ԭ�Ӱ뾶�Ĵ�С˳��rX��rY��rQ��rW | C��Ԫ��Q��Z���γ�QZ2�͵Ĺ��ۻ����� | D��X��Y������������ˮ����֮�䲻�ܷ�����Ӧ |
 Q��W��X��Y��Z��5�ֶ�����Ԫ�أ�ԭ������������Q�����ڱ���ԭ�Ӱ뾶��С��Ԫ�أ�Q��W��ɵĻ�������һ���������壬W��Y��X��Y��ɵĻ������ǻ������ų��Ĵ�����Ⱦ�Y��Z���γ�ԭ�Ӹ�����Ϊ1��1��1��2���������ӻ����
Q��W��X��Y��Z��5�ֶ�����Ԫ�أ�ԭ������������Q�����ڱ���ԭ�Ӱ뾶��С��Ԫ�أ�Q��W��ɵĻ�������һ���������壬W��Y��X��Y��ɵĻ������ǻ������ų��Ĵ�����Ⱦ�Y��Z���γ�ԭ�Ӹ�����Ϊ1��1��1��2���������ӻ����
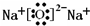
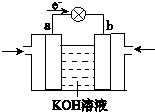
 Q��W��X��Y��Z��5�ֶ�����Ԫ�أ�ԭ������������W��Q��1��4�γɵĻ�����A��һ����Ҫ��Դ��W��Y��X��Y��ɵĻ������dz����Ĵ�����Ⱦ�Y��Z��1��1�γɵ����ӻ�����B����Ħ������Ϊ78g?mol-1����ش��������⣮
Q��W��X��Y��Z��5�ֶ�����Ԫ�أ�ԭ������������W��Q��1��4�γɵĻ�����A��һ����Ҫ��Դ��W��Y��X��Y��ɵĻ������dz����Ĵ�����Ⱦ�Y��Z��1��1�γɵ����ӻ�����B����Ħ������Ϊ78g?mol-1����ش��������⣮