题目内容
Fe2+和I-是两种常见的还原性离子。
(1)向FeSO4溶液中滴加氯水,溶液由浅绿色变成黄色,反应的离子方程式为???????????????? ;向KI溶液中滴加氯水,溶液由无色变成黄色,反应的离子方程式:?????????????????????? 。
(2)请以FeSO4溶液、KI溶液、氯水为试剂验证I-的还原性强于Fe2+。设计实验方案,补充完成实验步骤、预期现象和结论。其他限选试剂:3 mol·L-1 H2SO4、0.01 mol·L-1 KMnO4、20% KSCN、3%H2O2、淀粉溶液、紫色石蕊溶液。
实验步骤 | 预期现象与结论 |
步骤1:取2mLFeSO4溶液和2mLKI溶液混合于试管中,再滴加1~2滴氯水。 |
?????????????????????????? ; |
步骤2:____________________________________ ____________________________________。 |
|
(3)利用(2)提供的试剂证明碘与铁的化合物中铁显+2价,实验操作和现象是:取少量样品溶于水,?????????????????????????????????????????? 。
(1)2Fe2++Cl2=2Fe3++Cl-(3分) 2I-+Cl2=I2+2Cl-? (3分)
(2)(6分,各2分)
实验步骤 步骤1:………………………………………… | 预期现象与结论 溶液变成黄色 |
步骤2:向试管中继续滴加几滴20%KSCN溶液 或:向试管中继续滴加几滴淀粉溶液 | 溶液不变血红色,证明I-的还原性强于Fe2+ 或:溶液变蓝色,证明I-的还原性强于Fe2+ |
(3)滴加几滴20%KSCN溶液,无明显现象;再加入过量3%H2O2,溶液变血红色。(4分)
【解析】
试题分析:(1)硫酸亚铁中滴加强化性的氯水,亚铁离子被氧化为铁离子,所以发生溶液变色,所以离子方程式为2Fe2++Cl2=2Fe3++Cl-?? ;而往碘化钾溶液中同样滴加氯水,还原性的I-被氧化成碘单质,形成棕黄色的碘水溶液,所以离子方程式为2I-+Cl2=I2+2Cl-。
(2)本探究实验的目的是以FeSO4溶液、KI溶液、氯水为试剂验证I-的还原性强于Fe2+ 。要证明I-的还原性强于Fe2+ ,则可以设计让I-和Fe2+ 混合,然后滴加少量的强氧化剂,根据氧化还原规律,还原性强的先被氧化,所以滴加氯水试剂,只要证明先反应生成碘单质,而没有铁离子生成,即可得到结论。所以具体实验情况如下表:
实验步骤 步骤1:………………………………………… | 预期现象与结论 溶液变成黄色 |
步骤2:向试管中继续滴加几滴20%KSCN溶液 或:向试管中继续滴加几滴淀粉溶液 | 溶液不变血红色,证明I-的还原性强于Fe2+ 或:溶液变蓝色,证明I-的还原性强于Fe2+ |
(3)要证明碘与铁的化合物中铁显+2价,实质上就是利用(2)中提供的20%KSCN试剂来检验亚铁离子,所以正确的操作是:取少量样品溶于水,滴加几滴20%KSCN溶液,无明显现象;再加入过量3%H2O2,溶液变血红色,说明碘与铁的化合物中铁显+2价。
考点:本题考查的是氯水的强氧化性、围绕亚铁离子检验的探究性试验。

 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案Fe2+和I-是两种常见的还原性离子。
(1)向FeSO4溶液中滴加氯水,溶液由浅绿色变成黄色,反应的离子方程式为________________________;向KI溶液中滴加氯水,溶液由无色变成黄色,反应的离子方程式为______________________。
(2)请以FeSO4溶液、KI溶液、氯水、2% KSCN为试剂证明I-的还原性强于Fe2+。设计实验方案,补充完成实验步骤、预期现象和结论。
|
实验步骤 |
预期现象与结论 |
|
步骤1:取2mLFeSO4溶液和2mLKI溶液混合于试管中,再滴加1~2滴氯水。 |
现象:溶液变成黄色。 结论: 。 |
|
步骤2:__________________________ __________________________________ |
现象: ; 结论: |
(3)利用 中提供的试剂证明碘与铁的化合物中铁显+2价,实验操作和现象是:取少量样品溶于水, 。
(4)向含2mol FeI2 溶液中通入2.5mol Cl2 时,请写出总的离子方程式: 。
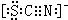 .
.


 Sx、CO+
Sx、CO+ Sx=COS、2COS+SO2=2CO2+
Sx=COS、2COS+SO2=2CO2+ Sx。其中COS中“C”化合价为__________。
Sx。其中COS中“C”化合价为__________。