题目内容
相同质量的庚烷、1-庚烯、2-庚炔,在空气中完全燃烧生成CO2和水,需要空气的量正确是( )
| A、烷烃最多 | B、烯烃最多 |
| C、炔烃最多 | D、三者一样多 |
考点:化学方程式的有关计算
专题:烃及其衍生物的燃烧规律
分析:由C→CO2、2H→H2O,可知12g碳消耗32g氧气,而2g氢元素消耗16g氧气,故相同的C、H元素,H元素消耗氧气更多,则相同质量的烃,烃中H元素质量分数越大消耗氧气越大.
解答:
解:由C→CO2、2H→H2O,可知12g碳消耗32g氧气,而2g氢元素消耗16g氧气,故相同的C、H元素,H元素消耗氧气更多,则相同质量的烃,烃中H元素质量分数越大消耗氧气越大,
庚烷、1-庚烯、2-庚炔中庚烷中H元素质量分数最大,故相同质量的三者,庚烷消耗氧气最多,
故选A.
庚烷、1-庚烯、2-庚炔中庚烷中H元素质量分数最大,故相同质量的三者,庚烷消耗氧气最多,
故选A.
点评:本题考查化学方程式的有关计算,注意对方程式的理解与灵活应用,难度不大.

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、22.4 L 氢气中含有氢分子数目为NA | ||
| B、0.5mol Na2CO3中含有的Na+数目为 0.5 NA | ||
| C、常温常压下,14 g 氮气含有的原子数目为 NA | ||
D、0.5 mol/L Fe2(SO4)3溶液中,S
|
如图所示是短周期元素A、B、C在周期表中的位置,A、C两种元素的原子核外电子数之和等于B原子的核电荷数.下列说法正确的是( )
| A | C | |
| B |
| A、元素A和C的氢化物分子之间都存在氢键 |
| B、C原子的最外层电子数为6 |
| C、元素B只存在一种氧化物 |
| D、元素A有多种可变的化合价 |
下列说法正确的是( )
| A、1molCO和1molN2所含分子数相等,质量相等,它们所占的体积也相等 |
| B、22.4LH2和71gCl2的物质的量相等 |
| C、非标准状况下,1mol任何气体的体积有可能是22.4L |
| D、1molHCl和1molH2O在标准状况下的体积都约是22.4L |
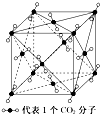 干冰晶体是一种面心立方结构,如图所示,即每8个CO2构成立 方体,且在6个面的中心又各有1个CO2分子,在每个CO2周围距离为
干冰晶体是一种面心立方结构,如图所示,即每8个CO2构成立 方体,且在6个面的中心又各有1个CO2分子,在每个CO2周围距离为
| ||
| 2 |
| A、4个 | B、8个 | C、12个 | D、6个 |
下表是某同学血常规检验报告单中的部分内容,该同学应注意补充的微量元素是( )
| 编号 | 项目 | 结果 | 正常范围参考值 | 单位 |
| 1 | 红细胞计数 | 2.1 | 3.5~5 | ×1012?L-1 |
| 2 | 血红蛋白 | 73 | 110~150 | g?L-1 |
| A、硒 | B、锌 | C、铁 | D、碘 |
下列叙述中,正确的是( )
| A、12g碳所含的碳原子数就是阿伏加德罗常数 |
| B、氦气的摩尔质量是8g |
| C、阿伏加德罗常数通常用NA表示,6.02×1023 mol-1称为阿伏加德罗常数 |
| D、4.4g二氧化碳气体中所含的原子个数与4.2g氮气中所含的原子个数相等 |
 某化工生产反应历程的能量变化如图,过程I没有使用催化剂,过程Ⅱ使用了催化剂,则可判断催化剂除了能改变反应速率外,还可以改变的是( )
某化工生产反应历程的能量变化如图,过程I没有使用催化剂,过程Ⅱ使用了催化剂,则可判断催化剂除了能改变反应速率外,还可以改变的是( )| A、反应物的熔沸点 |
| B、反应的完成程度 |
| C、生产能耗 |
| D、反应热效应 |