题目内容
现要配制500mL 1mol/L硫酸溶液,需用质量分数为98%,密度为1.84g/cm3的浓硫酸 mL.
考点:物质的量浓度的相关计算
专题:物质的量浓度和溶解度专题
分析:根据稀释定律及公式n=c?V和m=n?M求出硫酸的质量,溶质的质量÷质量分数=溶液的质量,溶液的体积由V=
计算.
| m |
| ρ |
解答:
解:n(H2SO4)=c?V=1mol/L×0.5L=0.5mol,m(H2SO4)=0.5mol×98g/mol=49g,
浓硫酸溶液的质量=
=50g,浓硫酸溶液的体积V=
=
=27.17ml,
故答案为:27.17.
浓硫酸溶液的质量=
| 49g |
| 98% |
| m |
| ρ |
| 50g |
| 1.84g/cm3 |
故答案为:27.17.
点评:本题考查稀释定律和n=c?V和m=n?M、V=
的联合计算,掌握解题思路是正确计算的关键,题目难度不大,注意计算的过程的严谨性和计算结果的准确性.
| m |
| ρ |

练习册系列答案
相关题目
在碳酸钠溶液中,c(Na+)与c(CO32-)的关系是( )
| A、c(Na+):c(CO32-)=1:1 |
| B、c(Na+):c(CO32-)>2:1 |
| C、c(Na+):c(CO32-)=2:1 |
| D、c(Na+):c(CO32-)<2:1 |


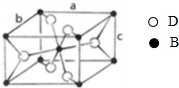 A、B、C、D四种元素的原子序数依次递增,A、B的基态原子中L层未成对电子数分别为3、2,C在短周期主族元素中电负性最小,D元素被称为继铁、铝之后的第三金属,其合金多用于航天工业,被誉为“21世纪的金属”,其基态原子外围电子占据两个能级且各能级电子数相等.请回答下列问题:
A、B、C、D四种元素的原子序数依次递增,A、B的基态原子中L层未成对电子数分别为3、2,C在短周期主族元素中电负性最小,D元素被称为继铁、铝之后的第三金属,其合金多用于航天工业,被誉为“21世纪的金属”,其基态原子外围电子占据两个能级且各能级电子数相等.请回答下列问题: