题目内容
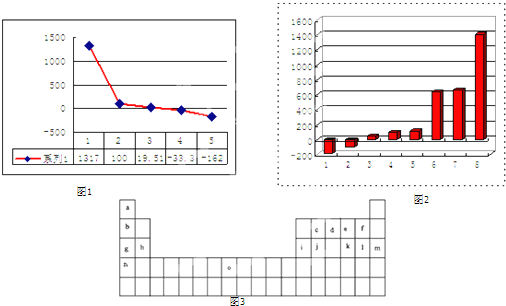
图3是元素周期表的一部分.表中所列的字母分别代表某一化学元素.
试回答下列问题
(1)元素“O”在周期表中的位置是 .
(2)画出“c”的简化电子排布式 .
(3)第三周期8种元素按单质熔点大小顺序的柱形图如图2,其中序列“1”代表 (填字母).
(4)b、c、d、e、f的氢化物的沸点(℃)直角坐标图如图1,序列“5”氢化物的化学式为: ;序列“1”氢化物的电子式为: .

试回答下列问题
(1)元素“O”在周期表中的位置是
(2)画出“c”的简化电子排布式
(3)第三周期8种元素按单质熔点大小顺序的柱形图如图2,其中序列“1”代表
(4)b、c、d、e、f的氢化物的沸点(℃)直角坐标图如图1,序列“5”氢化物的化学式为:
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:(1)元素“O”为Fe元素,处于第四周期第Ⅷ族;
(2)c为碳元素元素,核外电子数为7,根据能量最低原理书写核外电子排布式;
(3)第三周期8种元素单质中,只有Ar的熔点最低;
(4)b、c、d、e、f分别为Li、C、N、O、F,由氢化物的沸点(℃)直角坐标图可知,序号5沸点最低为甲烷,LiH属于离子化合物,沸点最高,与序号1对应.
(2)c为碳元素元素,核外电子数为7,根据能量最低原理书写核外电子排布式;
(3)第三周期8种元素单质中,只有Ar的熔点最低;
(4)b、c、d、e、f分别为Li、C、N、O、F,由氢化物的沸点(℃)直角坐标图可知,序号5沸点最低为甲烷,LiH属于离子化合物,沸点最高,与序号1对应.
解答:
解:(1)元素“O”为Fe元素,处于第四周期第Ⅷ族,故答案为:第四周期第Ⅷ族;
(2)c为碳元素元素,核外电子数为7,简化电子排布式为:[He]2s22p2,故答案为:[He]2s22p2;
(3)第三周期8种元素单质中,只有氯气、Ar为气体,氯气的相对分子质量大于Ar,Ar的熔点最低,图3中m为Ar,故答案为:m;
(4)b、c、d、e、f分别为Li、C、N、O、F,氢化物的沸点中LiH最大,甲烷最小,由氢化物的沸点(℃)直角坐标图可知,序列“5”的氢化物为CH4,序号1为LiH,电子式为 ,
,
故答案为:CH4; .
.
(2)c为碳元素元素,核外电子数为7,简化电子排布式为:[He]2s22p2,故答案为:[He]2s22p2;
(3)第三周期8种元素单质中,只有氯气、Ar为气体,氯气的相对分子质量大于Ar,Ar的熔点最低,图3中m为Ar,故答案为:m;
(4)b、c、d、e、f分别为Li、C、N、O、F,氢化物的沸点中LiH最大,甲烷最小,由氢化物的沸点(℃)直角坐标图可知,序列“5”的氢化物为CH4,序号1为LiH,电子式为
 ,
,故答案为:CH4;
 .
.
点评:本题考查位置结构性质关系应用,注意把握元素周期表和元素周期律,(4)为解答的难点,注意掌握物质熔沸点高低比较,题目难度不大,注重基础知识的考查.

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案
相关题目
等物质的量的下列有机物完全燃烧,消耗O2最多的是( )
| A、CH4 |
| B、CH3CH3 |
| C、C2H2 |
| D、C5H12 |
下列各组离子一定能大量共存的是( )
| A、含有大量Ba2+的溶液中:Cl、K+、SO42-、CO32- |
| B、含有大量H+的溶液中:Mg2+、Na+、HCO3-、SO42- |
| C、含有大量OH-的溶液中:NH4+、NO3、SO42-、CO32- |
| D、含有大量Na+的溶液中:H+、K+、SO42-、NO3- |
下列哪种方法不能增大铁跟盐酸反应的速率( )
| A、用粉末状铁代替块状铁 |
| B、用1mol?L-1HCl代替0.1mol?L-1HCl |
| C、增大压强 |
| D、改用不纯的铁代替纯铁 |
 已知:H2(g)+
已知:H2(g)+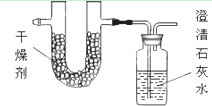 某烃CxHy同温同压条件下测得其蒸汽的密度是H2的43倍;将a g该烃完全燃烧,并使产生的产物全部依次通过下图装置,得到下表所列的实验结果(假设产生的气体产物完全被吸收).
某烃CxHy同温同压条件下测得其蒸汽的密度是H2的43倍;将a g该烃完全燃烧,并使产生的产物全部依次通过下图装置,得到下表所列的实验结果(假设产生的气体产物完全被吸收).