题目内容
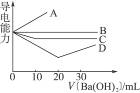
向20 mL 0.5 mol·L-1(NH4)2SO4溶液中逐滴加入0.5 mol·L-1 Ba(OH)2溶液,整个滴加过程中混合溶液的导电能力的变化基本符合下图中的( )
D 解析:溶液的导电能力的强弱与溶液中所含有的能自由移动的离子的浓度大小有关。 (NH4)2SO4和Ba(OH)2都是强电解质,在溶液中虽完全电离,但它们相互反应生成难电离的NH3·H2O和难溶的BaSO4,故滴加过程中,原溶液中的c(
![]() )和c(
)和c(![]() )均逐渐减小;当滴加Ba(OH)2溶液20 mL时,反应完全,离子浓度最小,溶液导电能力最弱;再继续滴加Ba(OH)2溶液,不再发生反应,随着Ba2+和OH-两种离子浓度的增大,溶液的导电能力逐渐增加。但由于后加入Ba(OH)2与原(NH4)2SO4的物质的量浓度相等(准确来说,应是电荷浓度相等),且受到恰好反应时所得40 mL稀氨水溶液的稀释,故最后得到溶液的导电能力应该比最初的20 mL 0.5 mol·L-1 (NH4)2SO4溶液的导电能力差。
)均逐渐减小;当滴加Ba(OH)2溶液20 mL时,反应完全,离子浓度最小,溶液导电能力最弱;再继续滴加Ba(OH)2溶液,不再发生反应,随着Ba2+和OH-两种离子浓度的增大,溶液的导电能力逐渐增加。但由于后加入Ba(OH)2与原(NH4)2SO4的物质的量浓度相等(准确来说,应是电荷浓度相等),且受到恰好反应时所得40 mL稀氨水溶液的稀释,故最后得到溶液的导电能力应该比最初的20 mL 0.5 mol·L-1 (NH4)2SO4溶液的导电能力差。 练习册系列答案
练习册系列答案
新课程新教材导航学系列答案
天天5分钟计算题系列答案
新概念英语单元测试AB卷系列答案
阳光课堂人民教育出版社系列答案
学业质量模块测评系列答案
新课标培优专项通专项训练系列答案
同步阅读训练系列答案
学业测评名校期末卷系列答案

桂壮红皮书题优练与测系列答案
相关题目