题目内容
已知:2H2S(g)+O2(g)=2S(s)+2H2O(l)△H=-aKJ/mol;
2H2S(g)+3O2(g)=2SO2(g)+2H2O(l)△H=-2bKJ/mol
则H2S与SO2两种气体转化为固体硫的热化学方程式为: .
2H2S(g)+3O2(g)=2SO2(g)+2H2O(l)△H=-2bKJ/mol
则H2S与SO2两种气体转化为固体硫的热化学方程式为:
考点:热化学方程式
专题:化学反应中的能量变化
分析:依据热化学方程式和盖斯定律计算得到反应热,注意热化学方程式的书写方法应用.
解答:
解:①2H2S(g)+O2(g)═2S(s)+2H2O(l),△H=-akJ/mol;
②2H2S(g)+3O2(g)═2SO2(g)+2H2O(l),△H=-2bkJ/mol;
依据盖斯定律①×3-②得到:4H2S(g)+2SO2(g)═6S(s)+4H2O(l),△H=+(2b-3a) kJ/mol
则H2S与SO2气体混合生成固体硫和液态水的热化学方程式:2H2S(g)+SO2(g)═3S(s)+2H2O(l),△H=+
(2b-3a)kJ/mol=+(b-1.5a)kJ/mol,
故答案为:2H2S(g)+SO2(g)═3S(s)+2H2O(l),△H=+(b-1.5a)kJ/mol.
②2H2S(g)+3O2(g)═2SO2(g)+2H2O(l),△H=-2bkJ/mol;
依据盖斯定律①×3-②得到:4H2S(g)+2SO2(g)═6S(s)+4H2O(l),△H=+(2b-3a) kJ/mol
则H2S与SO2气体混合生成固体硫和液态水的热化学方程式:2H2S(g)+SO2(g)═3S(s)+2H2O(l),△H=+
| 1 |
| 2 |
故答案为:2H2S(g)+SO2(g)═3S(s)+2H2O(l),△H=+(b-1.5a)kJ/mol.
点评:本题考查了盖斯定律的应用和热化学方程式的书写,题目难度不大,注意对盖斯定律概念的把握.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列有关化学用语正确的是( )
①乙烯的最简式C2H4
②乙醛的结构简式CH3COH
③四氯化碳的电子式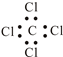
④乙烷的结构式CH3CH3.
①乙烯的最简式C2H4
②乙醛的结构简式CH3COH
③四氯化碳的电子式

④乙烷的结构式CH3CH3.
| A、全对 | B、全错 | C、①② | D、③④ |
分类是化学研究中常用的方法.下列分类方法正确的是( )
| A、根据溶液酸碱性,将化合物分为酸、碱、盐 |
| B、根据分散质微粒直径大小,将分散系分为胶体、浊液和溶液 |
| C、根据元素组成,将物质分为纯净物和混合物 |
| D、根据溶液导电性强弱,将电解质分为强电解质和弱电解质 |
可逆反应A(s)+3B(g)?2C(g)+D(g)在2L的密闭容器中反应,10min后,C的物质的量增加了0.6mol,则该反应的平均速率表示正确的是( )
| A、vA=0.03mol?L-1?min-1 |
| B、vB=0.045 mol?L-1?min-1 |
| C、vC=0.06mol?L-1?min-1 |
| D、vD=0.03 mol?L-1?min-1 |
在标准状况下,由两种气态烃组成的某混合气体2.24L完全燃烧后,得到3.36L二氧化碳和3.6g水,则两种气态烃可能是( )
| A、CH4和C3H8 |
| B、CH4和C3H4 |
| C、C2H6和C3H4 |
| D、C2H2和C2H4 |

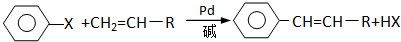 (X为卤原子,R为取代基)
(X为卤原子,R为取代基)