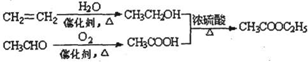题目内容
在三个烧杯中分别盛有海水,依次插入 (1)铁片;(2)导线相连的铜、铁片;(3)导线相连的锌、铁片,铁被腐蚀的速度由快到慢的顺序是( )
| A、(2)(1)(3) |
| B、(2)(3)(1) |
| C、(1)(2)(3) |
| D、(3)(2)(1) |
考点:金属的电化学腐蚀与防护
专题:电化学专题
分析:先判断发生腐蚀的类型,电化学腐蚀的速率大于化学腐蚀的速率,形成原电池时作负极被腐蚀,作正极被保护.
解答:
解:各组金属均有导线相连,并插入稀H2SO4液体中,
(1)没有构成原电池,发生化学腐蚀;
(2)Cu-Fe构成原电池,Fe作负极被腐蚀;
(3)Fe-Zn 构成原电池,Fe作正极被保护;
所以铁被腐蚀由快到慢的顺序是(2)>(1)>(3);
故选A.
(1)没有构成原电池,发生化学腐蚀;
(2)Cu-Fe构成原电池,Fe作负极被腐蚀;
(3)Fe-Zn 构成原电池,Fe作正极被保护;
所以铁被腐蚀由快到慢的顺序是(2)>(1)>(3);
故选A.
点评:本题考查了金属的腐蚀与防护,难度不大,不同条件下金属腐蚀的快慢:电解原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀>有防护腐蚀措施的腐蚀.

练习册系列答案
相关题目
氮的多样性主要体现在含氮化合物及其性质的多样性上,下列说法正确的是( )
| A、Fe2+、Mg2+、Cl-、NO3-能大量共存于pH=0的溶液中 |
| B、1L浓度为l mol?L-1的NH4Cl溶液中含有NA个NH4+ |
| C、除去NO中混有的少量NO2,可将混合气体通过盛有水的洗气瓶,再用排空气法收集NO |
| D、不论是浓硝酸还是稀硝酸,与铜反应均体现出硝酸的酸性和强氧化性 |
氧气的摩尔质量为( )
| A、32g |
| B、32mol |
| C、32 |
| D、32 g/mol |
下列化合物属于有机物的是( )
| A、碳酸 |
| B、尿素 |
| C、CaC2 |
| D、NH4CNO |
A、B、C、D四种金属,将AB用导线连接后,浸在稀硫酸中,在A上有氢气放出,而B溶解;当活泼金属浸在含有A和C两种金属离子可溶性盐溶液里时,在活泼金属上先析出C,把D放入B的硝酸盐溶液中,则D表面有B析出.这四种金属的活动性由强到弱的顺序是( )
| A、A>B>C>D |
| B、D>B>A>C |
| C、D>C>B>A |
| D、D>B>C>A |
按分散质微粒大小不同可将分散系分为胶体、溶液和浊液,胶体微粒大小为( )
| A、0.01nm~1nm |
| B、0.1nm~10nm |
| C、1nm~100nm |
| D、10nm~1000nm |

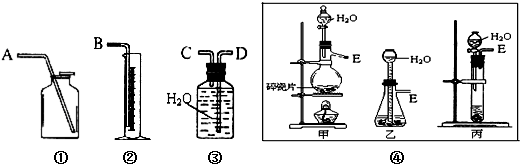
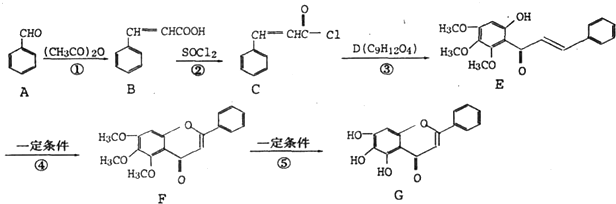
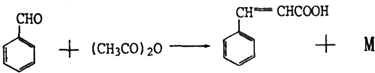
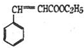 可作为果味香精.请设计合理方案以
可作为果味香精.请设计合理方案以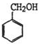 、CH3CH20H为原料合成
、CH3CH20H为原料合成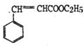 (用合成路线流程图表示,并注明反应条件).
(用合成路线流程图表示,并注明反应条件).