��Ŀ����
��14�֣�Q��W��X��Y��Z�����ڱ�ǰ36��Ԫ���е����ֳ���Ԫ�أ���ԭ��������������Wԭ������������������������֮��Ϊ3��4��Q��Y���������ǵ����������Ҫ���ʣ�X�ǵؿ��к�����ߵĽ���Ԫ�أ�Z���γɺ�ɫ����ש��ɫ����Z2O�ͺ�ɫ��ZO�������������������л�ѧ����ش�
 ��1��Q���ʵĵ���ʽΪ_______��
��1��Q���ʵĵ���ʽΪ_______�� W��X��Y�����Ӱ뾶�ɴ�С��˳��Ϊ____�������ӷ��Żش𣩡�
W��X��Y�����Ӱ뾶�ɴ�С��˳��Ϊ____�������ӷ��Żش𣩡�
 ��2��X��Y��ɵĻ��������ˮ�з�Ӧ�Ļ�ѧ����ʽ��______________________________��
��2��X��Y��ɵĻ��������ˮ�з�Ӧ�Ļ�ѧ����ʽ��______________________________��
��3��Na2Y��Һ������Ũ���ɴ�С��˳��Ϊ____________________________________________��
 ��4��ZO�ڸ����±�Q�ļ���̬�⻯�ﻹԭΪZ���ʣ�д����Ӧ�Ļ�ѧ����ʽ____________��
��4��ZO�ڸ����±�Q�ļ���̬�⻯�ﻹԭΪZ���ʣ�д����Ӧ�Ļ�ѧ����ʽ____________��
��5��ZCl2��Һ�л���FeCl3����ʱ���ɼ���_____________�����Լ�������pH��_________���ٹ��ˡ���֪��Fe(OH)3��Ksp��10-35����ѧ����Ϊ��������Һ�е�����Ũ��С��1��10-5mol/Lʱ�������ʹ���ȫ��
��6����ҵ�Ͽ��ø���������Z2Y + O2��2Z + YO2��ұ������Z������1molZʱת��____mol���ӡ�
 ��1��Q���ʵĵ���ʽΪ_______��
��1��Q���ʵĵ���ʽΪ_______�� W��X��Y�����Ӱ뾶�ɴ�С��˳��Ϊ____�������ӷ��Żش𣩡�
W��X��Y�����Ӱ뾶�ɴ�С��˳��Ϊ____�������ӷ��Żش𣩡� ��2��X��Y��ɵĻ��������ˮ�з�Ӧ�Ļ�ѧ����ʽ��______________________________��
��2��X��Y��ɵĻ��������ˮ�з�Ӧ�Ļ�ѧ����ʽ��______________________________����3��Na2Y��Һ������Ũ���ɴ�С��˳��Ϊ____________________________________________��
 ��4��ZO�ڸ����±�Q�ļ���̬�⻯�ﻹԭΪZ���ʣ�д����Ӧ�Ļ�ѧ����ʽ____________��
��4��ZO�ڸ����±�Q�ļ���̬�⻯�ﻹԭΪZ���ʣ�д����Ӧ�Ļ�ѧ����ʽ____________����5��ZCl2��Һ�л���FeCl3����ʱ���ɼ���_____________�����Լ�������pH��_________���ٹ��ˡ���֪��Fe(OH)3��Ksp��10-35����ѧ����Ϊ��������Һ�е�����Ũ��С��1��10-5mol/Lʱ�������ʹ���ȫ��
��6����ҵ�Ͽ��ø���������Z2Y + O2��2Z + YO2��ұ������Z������1molZʱת��____mol���ӡ�
 ��1��
��1��
 (1��) S2-��O2-��Al3+��2�֣�
(1��) S2-��O2-��Al3+��2�֣� ��2��Al2S3 + 6H2O��2Al(OH)3��+ 3H2S����2�֣�
��2��Al2S3 + 6H2O��2Al(OH)3��+ 3H2S����2�֣���3��c(Na+)��c(S2-)��c(OH-)��c(HS-)��c(H+) ��2�֣�
 ��4��3CuO + 2NH3
��4��3CuO + 2NH3 3Cu + N2 + 3H2O ��2�֣�
3Cu + N2 + 3H2O ��2�֣���5��CuO(1��) pH��4 ��2�֣� ��6��3 ��2�֣�
���������Q��W��X��Y��Z�����ڱ�ǰ36��Ԫ���е����ֳ���Ԫ�أ���ԭ��������������Q��Y���������ǵ����������Ҫ���ʣ���Q�ǵ�Ԫ�أ�Y����Ԫ�ء�X�ǵؿ��к�����ߵĽ���Ԫ�أ����X����Ԫ�ء�Z���γɺ�ɫ����ש��ɫ����Z2O�ͺ�ɫ��ZO�������������Z��ͭԪ�ء�Wԭ������������������������֮��Ϊ3��4����ԭ���������ڵ�Ԫ������Ԫ��֮�䣬���W����Ԫ�أ���
 ��1�����������к��е������������ʵĵ���ʽΪ
��1�����������к��е������������ʵĵ���ʽΪ ��
�� ���Ӻ�����Ӳ���Խ�࣬���Ӱ뾶Խ���ں�������Ų���ͬ��������ԭ������ԽС���Ӱ뾶Խ����W��X��Y�����Ӱ뾶�ɴ�С��˳��ΪS2-��O2-��Al3+��
���Ӻ�����Ӳ���Խ�࣬���Ӱ뾶Խ���ں�������Ų���ͬ��������ԭ������ԽС���Ӱ뾶Խ����W��X��Y�����Ӱ뾶�ɴ�С��˳��ΪS2-��O2-��Al3+�� ��2��X��Y��ɵĻ�����������������ˮ��ˮ��Ӧ�����������������⣬�����ˮ�з�Ӧ�Ļ�ѧ����ʽ��Al2S3 + 6H2O��2Al(OH)3��+ 3H2S����
��2��X��Y��ɵĻ�����������������ˮ��ˮ��Ӧ�����������������⣬�����ˮ�з�Ӧ�Ļ�ѧ����ʽ��Al2S3 + 6H2O��2Al(OH)3��+ 3H2S������3��Na2S��Һ��������ˮ�⣬��Һ�Լ��ԣ�����Һ������Ũ���ɴ�С��˳��Ϊc(Na+)��c(S2-)��c(OH-)��c(HS-)��c(H+)��
 ��4��CuO�ڸ����±�������ԭΪͭ���ʣ��������Ļ�ԭ�����ǵ���������ԭ���غ㻹��ˮ���ɣ���Ӧ�Ļ�ѧ����ʽΪ3CuO + 2NH3
��4��CuO�ڸ����±�������ԭΪͭ���ʣ��������Ļ�ԭ�����ǵ���������ԭ���غ㻹��ˮ���ɣ���Ӧ�Ļ�ѧ����ʽΪ3CuO + 2NH3 3Cu + N2 + 3H2O��
3Cu + N2 + 3H2O����5�����ڳ���ʱ���������µ����ʣ���CuCl2��Һ�л���FeCl3����ʱ���ɼ���CuO����pH������Һ��������Ũ��Ϊ1��10-5mol/Lʱ����ʱ��Һ������������Ũ��Ϊ
 ��10��10mol/L������ҺpH����4��������յ���pH��4���ٹ��ˡ�
��10��10mol/L������ҺpH����4��������յ���pH��4���ٹ��ˡ���6������Cu2S + O2��2Cu +SO2��֪��ֻ����Ԫ�صĻ��ϼ۴ӣ�2�����ߵ���4�ۣ�ʧȥ6�����ӣ��������1molZʱת��3mol���ӡ�

��ϰ��ϵ�д�
�����Ŀ



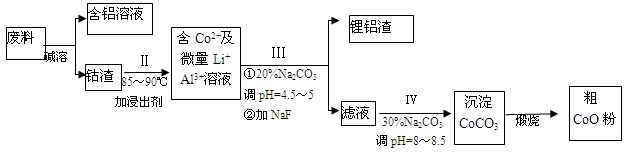
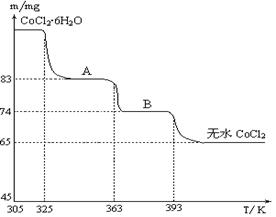
 (NxOy)�� H2O(��ƽʱx��y�þ�����ֵ��ʾ����������
(NxOy)�� H2O(��ƽʱx��y�þ�����ֵ��ʾ����������