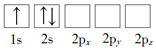
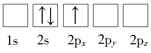
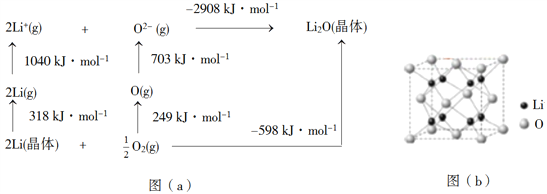
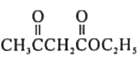题目内容
【题目】![]() 为阿伏加德罗常数的值。下列说法正确的是( )
为阿伏加德罗常数的值。下列说法正确的是( )
A. ![]() ,
,![]() 完全反应转移的电子数为
完全反应转移的电子数为![]()
B. 用电解粗铜的方法精炼铜,当电路中通过的电子数为![]() 时,阳极应有
时,阳极应有![]() 转化为
转化为![]()
C. 常温下,![]() 的
的![]() 溶液中,水电离出的
溶液中,水电离出的![]() 数为
数为![]()
D. ![]() 浓度为
浓度为![]() 的
的![]() 溶液中,阴离子数为
溶液中,阴离子数为![]()
【答案】A
【解析】
A. Mn元素的化合价由+7价降至+2价,则4mol![]() 完全反应转移电子物质的量为4mol×[(+7)-(+2)]=20mol,即转移电子数为20NA,A正确;
完全反应转移电子物质的量为4mol×[(+7)-(+2)]=20mol,即转移电子数为20NA,A正确;
B.电解精炼铜时,阳极为粗铜,阳极发生的电极反应有:比铜活泼的杂质金属失电子发生氧化反应以及Cu失电子的氧化反应:Cu-2e-=Cu2+,当电路中通过的电子数为NA时,即电路中通过1mol电子,Cu失去的电子应小于1mol,阳极反应的Cu的物质的量小于0.5mol,则阳极反应的Cu的质量小于0.5mol×64g/mol=32g,B错误;
C.溶液的体积未知,不能求出溶液中水电离出的H+数,C错误;
D.n(Na2CO3)=0.100mol/L×1L=0.100mol,由于![]() 发生水解:
发生水解:![]() +H2O
+H2O![]() +OH-、
+OH-、![]() +H2OH2CO3+OH-,故阴离子物质的量大于0.100mol,阴离子数大于0.100NA,D错误;
+H2OH2CO3+OH-,故阴离子物质的量大于0.100mol,阴离子数大于0.100NA,D错误;
答案选A。

【题目】下列实验中的颜色变化,与氧化还原反应无关的是( )
选项 | 实验操作 | 现象 |
A | AgNO3溶液滴入氯水中 | 产生白色沉淀,随后淡黄绿色逐渐褪去 |
B | FeCl3溶液滴入Mg(OH)2浊液中 | 白色浑浊转化为红褐色沉淀 |
C | H2C2O4溶液滴入KMnO4酸性溶液中 | 产生气泡,随后紫色褪去 |
D | Na块放在坩埚里并加热 | 发出黄色火焰,生成淡黄色固体 |
A.AB.BC.CD.D
【题目】现有部分元素的原子结构特点如表,下列叙述中正确的是( )
X | L层电子数是K层电子数的3倍 |
Y | 核外电子层数等于原子序数 |
Z | L层电子数是K层和M层电子数之和 |
W | 共用三对电子形成双原子分子,常温下为气体单质 |
A.W原子结构示意图为![]()
B.元素X和Y只能形成原子个数比为1∶2的化合物
C.元素X比元素Z的非金属性强
D.X、Y、Z、W四种元素不能形成离子化合物