题目内容
15.下列有关化学用语的表示错误的是( )| A. | 甲烷的比例模型: | B. | 氯离子的结构示意图: | ||
| C. | 溴原子的价层电子排布式:4s24p5 | D. | 过氧化钠的电子式: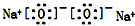 |
分析 A.比例模型能够体现出分子的空间结构及各原子相对体积大小,据此判断甲烷的比例模型;
B.氯离子的核电荷数为17,核外电子总数为18,最外层达到8电子稳定结构;
C.溴原子位于第四周期ⅤⅡA族,最外层含有7个电子,据此判断其价电子排布式;
D.过氧化钠为离子化合物,过氧根离子的表示方法错误.
解答 解:A.甲烷为正四面体结构,碳原子半径大于氢原子,则甲烷的比例模型为: ,故A正确;
,故A正确;
B.氯离子的核电荷数为17,核外电子总数为18,则氯离子正确的结构示意图为: ,故B正确;
,故B正确;
C.溴原子的价电子数为5,其价层电子排布式为:4s24p5,故C正确;
D.过氧化钠为离子化合物,钠离子直接用离子符号表示,过氧根离子需要标出所带电荷及最外层电子,过氧化钠正确的电子式为: ,故D错误;
,故D错误;
故选D.
点评 本题考查了常见化学用语的判断,题目难度中等,注意掌握电子式、离子结构示意图、比例模型与球棍模型等化学用语的表示方法,试题有利于培养学生规范答题的能力.

练习册系列答案
相关题目
1.NA表示阿伏伽德罗常数,下列说法正确的是( )
| A. | 0.2mol•L-1 Na2SO4溶液中含有0.4NA个Na | |
| B. | 在标准状况下,NA个C02分子与NA个H2SO4分子所占的体积之比为1:1 | |
| C. | 5.6g铁在足量氯气中燃烧时失去的电子数目为0.2NA | |
| D. | 常温常压下,64g SO2中含有的原子数为3NA |
3.现有四种元素的基态原子的电子排布式如下:①1s22s22p63s23p4;②1s22s22p63s23p3;③1s22s22p5;④1s22s22p63s23p2则下列有关比较中正确的是( )
| A. | 第一电离能:③>②>④>① | B. | 原子半径:①>②>④>③ | ||
| C. | 电负性:③>①>②>④ | D. | 最高正化合价:③>①>②>④ |
20.在正规考试化学试卷的试题前总有“可能用到的相对原子质量”一项,如H-1 C-12 Cl-35.5 N-14等.请问这些数据准确的说法应该是( )
| A. | 某种核素的相对原子质量 | |
| B. | 某种核素的质量数 | |
| C. | 某种元素所有核素质量数的平均值 | |
| D. | 某种元素的平均相对原子质量的近似值 |
4.下列有机物在常温下呈液态的是( )
| A. | CH3(CH2)4CH3 | B. | C18H38 | C. | C3H6 | D. | CH3Cl |
5.a、b、c、d是HCl、BaCl2、AgNO3、Na2CO3四种溶液中的一种,现将它们两两混合,现象如下表所示:
由上述现象可推知a、b、c、d依次是( )
| 反应物 | a+b | c+d | a+d | a+c | b+d |
| 现象 | 白色沉淀 | 白色沉淀 | 白色沉淀 | 白色沉淀 | 无色气体 |
| A. | AgNO3、HCl、Na2CO3、BaCl2 | B. | AgNO3、HCl、BaCl2、Na2CO3 | ||
| C. | BaCl2、Na2CO3、AgNO3、HCl | D. | HCl、BaCl2、AgNO3、Na2CO3 |
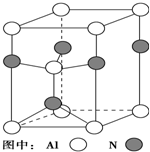 元素周期表中的第ⅢA、ⅣA、ⅤA族的部分元素往往易形成原子晶体,氮化铝、氮化硼、磷化硼和砷化镓属于此列,如氮化铝晶体晶胞如右图所示
元素周期表中的第ⅢA、ⅣA、ⅤA族的部分元素往往易形成原子晶体,氮化铝、氮化硼、磷化硼和砷化镓属于此列,如氮化铝晶体晶胞如右图所示
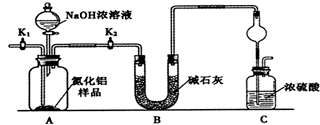
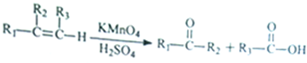 由
由 到
到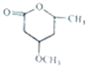 的合成路线如下所示:
的合成路线如下所示:
 ;B
;B ;C
;C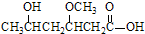 .
.