题目内容
5.下列有关金属钠的说法中,错误的是( )| A. | 钠应保存在煤油中 | |
| B. | 钠与氧气反应的产物与反应条件有关 | |
| C. | 钠在反应中易失去电子,表现出还原性 | |
| D. | 钠只有在加热条件下才能与氯气反 |
分析 A.钠的性质很活泼,易和水、氧气反应,钠应保存在煤油中;
B.钠性质活泼,可与氧气在没有条件下和加热条件下分别生成氧化钠、过氧化钠;
C.钠最外有1个电子,所以在化学反应中钠易失去电子;
D.在点燃条件下,钠能在氯气中燃烧.
解答 解:A.钠易和氧气、水反应,所以要密封保存,钠的密度大于煤油,且和煤油不反应,所以钠可以保存在煤油中,故A正确;
B.钠在没有条件下和氧气反应生成氧化钠,在点燃条件下,和氧气反应生成淡黄色的过氧化钠,故B正确;
C.钠最外有1个电子,所以在化学反应中钠易失去电子而表现出还原性,故C正确;
D.钠性质很活泼,在点燃条件下,钠能在氯气中燃烧,故D错误;
故选D.
点评 本题考查金属钠的有关知识,涉及钠的贮存、钠的性质等知识点,根据钠的结构分析其性质,注意相关基础知识的积累,难度不大.

练习册系列答案
相关题目
15.向密度为d g•cm-3的盐酸中逐滴加入硝酸银溶液到过量,生成沉淀的质量与原盐酸的质量相等,原盐酸的物质的量浓度为( )
| A. | 25.4d mol•L-1 | B. | 12.7d mol•L-1 | C. | 6.97d mol•L-1 | D. | 6.35d mol•L-1 |
16.下列物质中,发生消去反应生成的烯烃只有一种的是( )
①2丁醇
②2甲基2丙醇
③1丁醇
④2甲基2丁醇.
①2丁醇
②2甲基2丙醇
③1丁醇
④2甲基2丁醇.
| A. | ①② | B. | ②③ | C. | ②④ | D. | ③④ |
13.下列比较不正确的是( )
| A. | 非金属性:C>N | B. | 酸性:HClO4>H2CO3 | ||
| C. | 碱性:NaOH>Mg(OH)2 | D. | 热稳定性H2O>H2S |
20.下列各组离子,能在指定溶液中大量共存的是( )
| A. | 无色溶液中:Ba2+、HCO3-、NO3-、K+ | |
| B. | 能使紫色石蕊试剂变红的溶液中:NH4+、NO3-、CO32-、Na+ | |
| C. | 使酚酞试液变红的溶液:Na+、Ca2+、NO3-、Cl- | |
| D. | 有SO42-存在的溶液中:K+、Ba2+、Ag+、NO3- |
10.下列食物中属于酸性食物的是( )
| A. | 西红柿 | B. | 羊肉 | C. | 柠檬 | D. | 黄瓜 |
15.难溶电解质的溶解平衡属于动态平衡.已知几种难溶电解质的溶度积(25℃时,忽略溶液混合时的体积变化)如下表.
(1)常温下,将适量Li2CO3固体溶于水配成Li2CO3悬浊液,该悬浊液中c(Li+)=0.12mol•L-1,则c(CO32-)=
0.06mol/L
(2)一定温度下,将0.1molAgCl加入1L0.1mol•L-1Na2CO3溶液中,充分搅拌,写出该反应的离子方程式:2AgCl(s)+CO32-(aq)?Ag2CO3(s)+2Cl-(aq)溶液中$\frac{c(C{{O}^{2-}}_{3})}{{c}^{2}(C{l}^{-})}$为2.5×10-8
(3)常温下,向5ml含有KCl和KI浓度均为0.01mol•L-1的溶液中加入8mL0.01mol•L-1AgNO3溶液,此时溶液中溶质的离子浓度大小关系为c(K+)>c(NO3-)>c(Cl-)>c(Ag+)>c(I-).
| 化学式 | AgCl | Ag2CO3 | AgI | Li2CO3 |
| 溶度积(K甲 ) | 2×10-10 | 1×10-11 | 8.5×10-17 | 8.64×10-4 |
0.06mol/L
(2)一定温度下,将0.1molAgCl加入1L0.1mol•L-1Na2CO3溶液中,充分搅拌,写出该反应的离子方程式:2AgCl(s)+CO32-(aq)?Ag2CO3(s)+2Cl-(aq)溶液中$\frac{c(C{{O}^{2-}}_{3})}{{c}^{2}(C{l}^{-})}$为2.5×10-8
(3)常温下,向5ml含有KCl和KI浓度均为0.01mol•L-1的溶液中加入8mL0.01mol•L-1AgNO3溶液,此时溶液中溶质的离子浓度大小关系为c(K+)>c(NO3-)>c(Cl-)>c(Ag+)>c(I-).
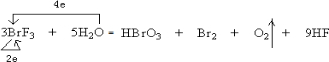 ,还原剂是H2O和BrF3,氧化剂是BrF3.氧化产物是HBrO3、O2. 还原产物是Br2(以上均填化学式)
,还原剂是H2O和BrF3,氧化剂是BrF3.氧化产物是HBrO3、O2. 还原产物是Br2(以上均填化学式)