题目内容
用Na2CO3固体配制一定物质的量浓度的Na2CO3溶液时,不需要使用的玻璃仪器是( )
| A、容量瓶 | B、玻璃棒 |
| C、漏斗 | D、烧杯 |
考点:不能加热的仪器及使用方法
专题:
分析:配制一定物质的量浓度的溶液步骤为:计算、称量(量取)、溶解、定容等,据此进行判断.
解答:
解:配制一定物质的量浓度的溶液步骤为:计算、称量(量取)、溶解、定容等,
A.配制一定物质的量浓度的溶液,一定用到容量瓶,故A错误;
B.溶解和转移需要使用玻璃棒,故B错误;
C.不需要使用漏斗,故C正确;
D.溶解需要使用烧杯,故D错误.
故选C.
A.配制一定物质的量浓度的溶液,一定用到容量瓶,故A错误;
B.溶解和转移需要使用玻璃棒,故B错误;
C.不需要使用漏斗,故C正确;
D.溶解需要使用烧杯,故D错误.
故选C.
点评:本题考查了配制一定物质的量浓度的溶液使用的仪器,注意铁架台不是玻璃仪器,本题难度不大.

练习册系列答案
相关题目
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )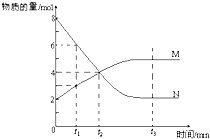

| A、反应的化学方程式为:N?2M |
| B、t2时,正逆反应速率相等,达到平衡 |
| C、t3时,正反应速率大于逆反应速率 |
| D、t1时,N的浓度是M浓度的2倍 |
下列有关说法正确的是( )
| A、若在海轮外壳上附着一些铜块,则可以减缓海轮外壳的腐蚀 |
| B、2NO(g)+2CO(g)=N2(g)+2CO2(g)在常温下能自发进行,则该反应的△H<0 |
| C、增大反应物浓度可加快反应速率,因此用浓硫酸与铁反应能增大生成H2的速率 |
| D、对于乙酸与乙醇的酯化反应(△H<0),加入少量浓硫酸并加热,该反应的反应速率和平衡常数均增大 |
2014年度诺贝尔化学奖授予了研制出超高分辨率荧光显微镜的三位科学家.该仪器可 用于研究细胞结构和功能等.则下列有关仪器分析说法中错误的是( )
| A、原子吸收光谱仪可用于测定物质中的金属元素 |
| B、质谱仪不能用于分析有机化合物的结构 |
| C、红外光谱仪可用于测定有机化合物的官能团 |
| D、氢核磁共振仪能鉴别CH3COOCH2CH3与CH3CH2COOCH3 |
下列各组物质中,不满足组内任意两种物质在一定条件下均能发生反应的是( )
 | 甲 | 乙 | 丙 |
| A | MgO | HCl | Al |
| B | Fe | O2 | S |
| C | HCl | NaOH | Ca(HCO3)2 |
| D | AlCl3 | NaOH | NaHCO3 |
| A、A | B、B | C、C | D、D |
已知100mL0.55mol?L-1氢氧化钠溶液与100mL0.5mol?L-1盐酸溶液混合放出热量为a kJ(a>0).下列说法正确的是( )
| A、氢氧化钠和盐酸反应的中和热为a kJ |
| B、若其他条件不变,盐酸体积换成200 mL,则中和热为原来的2倍 |
| C、若其他条件不变,将氢氧化钠溶液换成200 mL,则放出热量2a kJ |
| D、若其他条件不变,将盐酸浓度换成0.55mol?L-1,则中和热不变 |
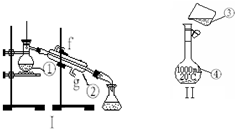 掌握仪器的名称、组装及使用方法是中学化学实验的基础,如图为两套实验装置.
掌握仪器的名称、组装及使用方法是中学化学实验的基础,如图为两套实验装置. 用图表示的一些物质或概念间的从属关系中正确的是( )
用图表示的一些物质或概念间的从属关系中正确的是( )