题目内容
10.北京时间11月1日清晨5时58分07秒,中国“长征二号F”遥八运载火箭在酒泉卫星发射中心载人航天发射场点火发射,火箭的第三级使用的推进剂是液氢和液氧.已知下面在298K时的热化学方程式:
2H2(g)+O2(g)═2H2O(l);△H═-571.6kJ•mol-1
CH4(g)+2O2(g)═CO2(g)+2H2O(l);△H═-890.3kJ•mol-1
C(S)+O2(g)═CO2(g);△H═-393.5kJ•mol-1
根据上面的热化学方程式完成下列问题:
(1)通过计算说明等质量的H2、C、CH4完全燃烧时放出热量最多的是H2.
(2)根据以上反应,则C(s)+2H2(g)═CH4(g)的焓变△H=-74.8kJ•mol-1.
(3)已知H2O(l)═H2O(g);△H═+44.0kJ•mol-1
试写出甲烷燃烧生成二氧化碳和水蒸气时的热化学方程式:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-802.3 kJ•mol-1.
分析 (1)根据热化学方程式的含义分别计算出1克物质燃烧释放出的热量;
(2)根据盖斯定律,由已知热化学方程式乘以适当的系数进行加减,反应热也处于相应的系数进行相应的加减,构造目标热化学方程式,从而得出化学反应的焓变;
(3)根据盖斯定律,由已知热化学方程式乘以适当的系数进行加减,反应热也处于相应的系数进行相应的加减,构造目标热化学方程式;
解答 解:(1)设H2、C、CH4的质量都为1g,完全燃烧时放出热量分别是$\frac{571.6kJ}{4}$、$\frac{393.5kJ}{12}$、$\frac{890.3kJ}{16}$、最大值应为$\frac{571.6kJ}{4}$,因此相同质量的H2、C、CH4完全燃烧时,放出热量最多的是H2;
故答案为:H2;
(2)①2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ•mol-1?
②CH4(g)+2O2(g)═CO2(g)+2H2O (l)△H=-890.3kJ•mol-1?
③C(s)+O2(g)═CO2(g)△H=-393.5kJ•mol-1?
根据盖斯定律,①+③-②得热化学方程式为C(s)+2H2(g)═CH4(g)△H=-74.8 kJ•mol-1;
故答案为:-74.8 kJ•mol-1;?
(3)①CH4(g)+2O2(g)═CO2(g)+2H2O (l)△H=-890.3kJ•mol-1?
②H2O(l)═H2O(g)△H=+44.0kJ•mol-1
根据盖斯定律,①+②×2得:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-802.3 kJ•mol-1;
故答案为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-802.3 kJ•mol-1;
点评 本题考查反应热的计算,涉及盖斯定律的应用,题目难度不大,对学生的综合计算能力要求较高.

 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案(1)按物质的分类方法填写表格的空白处 (填编号):
| 分类标准 | 能导电的物质 | 电解质 | 非电解质 |
| 属于该类的物质 | ②⑦⑧⑨⑩ | ①③⑤⑥⑩ | ④⑪ |
(3)将⑨滴加到⑦中至过量的实验现象是先产生沉淀后溶解.
(4)将③通入⑧中至恰好完全反应,则溶液导电能力的变化为导电能力逐渐增强.
| A. | 3:2:2 | B. | 1:2:3 | C. | 1:3:3 | D. | 3:1:1 |
①加入AgNO3溶液
②加入NaOH溶液
③加热
④加蒸馏水
⑤加入硝酸至溶液呈酸性
⑥加入NaOH乙醇溶液.
| A. | ②③⑤① | B. | ①②③④ | C. | ④②⑤③ | D. | ⑥③①⑤ |
| A. | $\frac{ac}{22400}$mol•L-1 | B. | $\frac{a}{22.4b}$mol•L-1 | ||
| C. | $\frac{ac}{22400b+36.5}$mol•L-1 | D. | $\frac{1000ac}{22.4b+36.5a}$mol•L-1 |
| A. | 干冰升华和液氯气化时要破坏不同的微粒间作用力 | |
| B. | CO2和SiO2具有相同的化学键类型和晶体类型 | |
| C. | 水结成冰体积膨胀、密度变小,这一事实与水分子间存在氢键有关 | |
| D. | 盐酸能电离出氢离子和氯离子,所以HCl中存在离子键 |
| A. | 10 s | B. | 12 s | C. | 大于12 s | D. | 小于12 s |
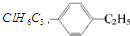 表示的有机物中,能发生消去反应的卤代烃共有( )
表示的有机物中,能发生消去反应的卤代烃共有( )| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
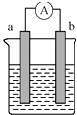 如图是某化学兴趣小组探究不同条件下化学能转化为电能的装置.请回答下列问题.
如图是某化学兴趣小组探究不同条件下化学能转化为电能的装置.请回答下列问题.