题目内容
4.(1)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O.(2)在以上中性溶液中继续滴加Ba(OH)2溶液,请写出此步反应的离子方程式:Ba2++SO42-=BaSO4↓.
(3)现有m g某气体,它由双原子分子构成,它的摩尔质量为M g•mol-1.若阿伏加德罗常数用NA表示,则:
①该气体(不与水反应)溶于1L水中,其溶液中溶质的质量分数为$\frac{m}{(m+1000)}$×100%.
②该气体溶于水后形成V L溶液,则该溶液溶质的物质的量浓度为$\frac{m}{MV}$mol/L.
分析 (1)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性,NaHSO4和Ba(OH)2按照2:1反应生成硫酸钡、硫酸钠和水,以此书写离子方程式;
(2)至中性时溶液中溶质只有Na2SO4,加入Ba(OH)2溶液生成BaSO4沉淀;
(3)①溶于1L水中,溶液质量为(m+1000)g,溶质质量为m g,溶液质量分数=$\frac{溶质质量}{溶液质量}$×100%;
②根据c=$\frac{n}{V}$计算溶液物质的量浓度.
解答 解:(1)NaHSO4是二元强酸的酸式盐,可以理解为全部电离.当反应后溶液呈中性时,其反应式为:2NaHSO4+Ba(OH)2=BaSO4↓+Na2SO4+2H2O,离子反应方程式为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,
故答案为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O;
(2)此时溶液中溶质只有Na2SO4,加入Ba(OH)2的离子反应方程式为:Ba2++SO42-=BaSO4↓,
故答案为:Ba2++SO42-=BaSO4↓;
(3)①溶于1L水中,溶液质量为(m+1000)g,溶质质量为m g,溶质的质量分数为$\frac{m}{(m+1000)}$×100%,
故答案为:$\frac{m}{(m+1000)}$×100%;
②该气体溶于水后形成VL溶液,其溶液的物质的量浓度为 $\frac{\frac{m}{M}mol}{VL}$=$\frac{m}{MV}$mol/L,故答案为:$\frac{m}{MV}$.
点评 本题考查了离子反应和离子方程式的书写、物质的量、溶液浓度有关计算,熟悉基本计算公式即可解答,题目难度不大,侧重于考查学生的分析能力和计算能力.

练习册系列答案
相关题目
14.下列A、B两种元素的原子序数,其中可以组成AB2型离子化合物的( )
| A. | 6和8 | B. | 19和16 | C. | 12和17 | D. | 7和8 |
12.化学与社会、生产、生活密切相关.下列说法不正确的是( )
| A. | 我国古代文献《天工开物》记载“凡研硝(KNO3)不以铁碾入石臼,相激火生,祸不可测”是因为KNO3能自燃 | |
| B. | 用纯碱溶液和盐酸可以清洗锅炉中的硫酸钙 | |
| C. | 制造新版人民币所用的棉花、优质针叶木等原料的主要成分是纤维素 | |
| D. | 运用荧光蛋白可以观测到细胞的活动,荧光蛋白是一种高分子化合物且能发生水解 |
19.下列离子组一定能够大量共存的是( )
| A. | 含ClO-的溶液中:Fe3+、S042-、NO3-、K+ | |
| B. | 使石蕊试液显红色的溶液中:Fe2+、K+、NO3-、CI- | |
| C. | 在c(H+):c(OH-)=1:1012的溶液中,Na+、I-、NO3-、SO42- | |
| D. | 能使有色布条褪色的溶液:K+、S032-、NO3-、Mg2+ |
9.下列物质放入水中,能形成溶液的是( )
| A. | 面粉 | B. | 牛奶 | C. | 白糖 | D. | 植物油 |
16.下列物质对应的电子式书写正确的是( )
| A. | NH4Br: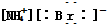 | B. | CaCl2: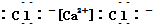 | ||
| C. | Na2O2: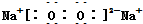 | D. | N2:N??N |
14.硼砂晶体由Na+、Xm-和H2O构成,它们之间存在的作用力有( )
| A. | 离子键 | B. | 共价键 | C. | 金属键 | D. | 范德华力 | ||||
| E. | 氢键 |
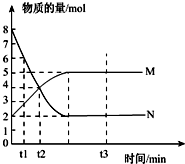 (1)一定温度下,在容积为V L的密闭容器中进行反应:aN(g)?bM(g),M、N的物质的量随时间的变化曲线如图所示:
(1)一定温度下,在容积为V L的密闭容器中进行反应:aN(g)?bM(g),M、N的物质的量随时间的变化曲线如图所示: