题目内容
已知A、B、C、D和E 5种分子所含原子的数目依次为1、2、3、4和6,且都含有18个电子。又知B、C和D是由两种元素的原子组成。请回答:
(1)组成A分子的原子的核外电子排布式是___________;
(2)B和C的分子式分别是___________和___________;C分子的立体结构呈___________形,该分子属于___________分子(填“极性”或“非极性”);
(3)若向D的稀溶液中加入少量二氧化锰,有无色气体生成。则D的分子式是___________,该反应的化学方程式为___________;
(4)若将1 mol E在氧气中完全燃烧,只生成1 mol CO2和2 mol H2O,则E的分子式是___________。
(1)1S22S22P63S23P6
(2)HCl H2S V 极性
(3)H2O2; 2 H2O2 ![]() 2H2O+O2↑
2H2O+O2↑
(4)CH4O(答CH3OH不扣分)
解析:
题目中给出已知五种分子中原子数依次为1,2,3,4,6,且均含18电子,B、C 和D由两元素组成。
单原子分子中含18电子的为Ar原子、核外电子排布为1S22S22P63S23P6
双原子分子、三原子分子(B和C)为HCl和H2S,H2S的分子立体结构为V型,属于极性分子。
如果只考虑D为两种元素的原子组成4原子分子,可以为PH3和H2O2,与MnO2反应产生无色气体的为H2O2,化学方程式为
2 H2O2 ![]() 2H2O+O2↑
2H2O+O2↑
如果只考虑六原子含18电子的分子可以是N2H4和CH4O,题目要求1molE在O2中完全燃烧,只生成1molCO2和2molH2O,显然E 的分子式应为CH4O(甲醇)。

练习册系列答案
相关题目
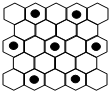 已知A、B、C、D和E都是元素周期表中前20号的元素,它们的原子序数依次增大.A原子的价电子层的p轨道中只有1个电子;B、C、D元素的基态原子具有相同的能层数,B、D元素的原子的p能级上都有1个未成对电子,D原子得一个电子填入3p轨道后,3p轨道已充满,C原子的p轨道中有3个未成对电子;E是同周期第一电离能最小的元素.回答下列问题:
已知A、B、C、D和E都是元素周期表中前20号的元素,它们的原子序数依次增大.A原子的价电子层的p轨道中只有1个电子;B、C、D元素的基态原子具有相同的能层数,B、D元素的原子的p能级上都有1个未成对电子,D原子得一个电子填入3p轨道后,3p轨道已充满,C原子的p轨道中有3个未成对电子;E是同周期第一电离能最小的元素.回答下列问题:
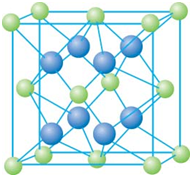 已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大.A与其他4种元素既不在同一周期又不在同一主族.B和C属同一主族,D和E属同一周期,又知E是周期表中1-18列中的第7列元素.D的原子序数比E小5,D跟B形成的晶体其晶胞结构如图,图中小球代表D,大球代表B.请回答:
已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大.A与其他4种元素既不在同一周期又不在同一主族.B和C属同一主族,D和E属同一周期,又知E是周期表中1-18列中的第7列元素.D的原子序数比E小5,D跟B形成的晶体其晶胞结构如图,图中小球代表D,大球代表B.请回答: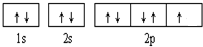
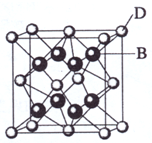 (2009?海南)已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大.A与其他4种元素既不在同一周期又不在同一主族.B和C属同一主族,D和E属同一周期,又知E是周期表中1-18列中的第7列元素.D的原子序数比E小5,D跟B可形成离子化合物其晶胞结构如右图.
(2009?海南)已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大.A与其他4种元素既不在同一周期又不在同一主族.B和C属同一主族,D和E属同一周期,又知E是周期表中1-18列中的第7列元素.D的原子序数比E小5,D跟B可形成离子化合物其晶胞结构如右图.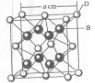 (2011?开封一模)[化学--选修物质结构与性质]
(2011?开封一模)[化学--选修物质结构与性质]