题目内容
12.下列实验能取得预期结论或结果的是( )| A. | 制备AlCl3晶体:将AlCl3溶液加热、蒸干,并灼烧 | |
| B. | 证明某卤代烃中的碘原子:在卤代烃中滴加NaOH溶液,振荡后滴加AgNO3溶液 | |
| C. | 鉴别乙醇、乙醛、乙酸三种物质的水溶液:用新制碱性氢氧化铜悬浊液 | |
| D. | 检验甲酸中混有甲醛:可先向样品中加入足量NaOH溶液中和甲酸,再进行银镜反应实验 |
分析 A.氯化铝是强酸弱碱盐,铝离子水解生成HCl,生成的HCl水溶液以挥发,升高温度促进其挥发,所以蒸干溶液得到氢氧化铝固体,灼烧氢氧化铝固体分解生成氧化铝;
B.加入硝酸银溶液前需要用稀硝酸中和NaOH,否则氢氧根离子与银离子反应,干扰了检验结果;
C.加入新制Cu(OH)2悬浊液,乙醇不反应,乙醛在加热时生成砖红色沉淀,乙酸和氢氧化铜发生中和反应;
D.甲酸钠和甲醛中都含有醛基,都能发生银镜反应.
解答 解:A.AlCl3在加热时水解生成Al(OH)3和HCl,HCl易挥发,蒸干灼烧得到的是Al2O3,无法获得AlCl3晶体,故A错误;
B.证明某卤代烃中的碘原子:在卤代烃中滴加NaOH溶液加热,冷却后加入稀硝酸中和氢氧化钠,振荡后再滴加AgNO3溶液,否则氢氧根离子与银离子反应,干扰了卤素离子的检验,故B错误;
C.加入新制Cu(OH)2悬浊液,乙醇不反应,乙醛在加热时生成砖红色沉淀,乙酸和氢氧化铜发生中和反应,氢氧化铜溶解,现象不同,所以可以鉴别,故C正确;
D.甲酸钠和甲醛中都含有醛基,都能发生银镜反应,所以用足量氢氧化钠溶液和银氨溶液不能鉴别二者,故D错误;
故选C.
点评 本题考查了实验方案评价,明确实验原理是解本题关键,根据物质的性质来分析解答,注意掌握卤代烃中卤元素的检验方法、物质的检验等知识点,易错选项是B,检验卤代烃中的卤元素时要注意水解后先中和碱,为易错点.

练习册系列答案
相关题目
3.下列离子方程式正确的是( )
| A. | 碳酸钙溶于醋酸:CaCO3+2H+=Ca2++CO2↑+H2O | |
| B. | 用烧碱溶液吸收氯气:Cl2+2OH-=Cl-+ClO-+H2O | |
| C. | NH4HSO4溶液与过量NaOH稀溶液反应:NH4++OH-=NH3•H2O | |
| D. | FeBr2溶液中通入少量Cl2:2Fe2++2Br-+Cl2=2Fe3++Br2+2Cl- |
4.下列变化中,需要加入适当的氧化剂才能完成的是( )
| A. | Fe→FeCl3 | B. | CuO→Cu | C. | SO3→H2SO4 | D. | HNO3→NO |
7.用固体配制一定物质的量浓度的溶液时,其操作要领包括:①溶解;②定容;③摇匀;④计算;⑤称量等方面,其正确的操作是( )
| A. | ④⑤①②③ | B. | ④⑤③②① | C. | ①②③④⑤ | D. | ②①③⑤④ |
17.以下物质可以通过化合反应直接制得的是( )
| A. | Al(OH)3 | B. | Fe(OH)3 | C. | Fe(OH)2 | D. | H2SiO3 |
19.在标准状况下,与32gO2的体积相等的N2为( )
| A. | 质量为14g | B. | 分子数为6.02×1023 | ||
| C. | 体积为11.2L | D. | 物质的量为2mol |
 .
.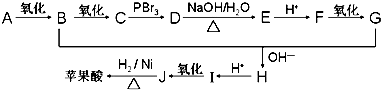


 +n HO-CH2CH2-OH$\stackrel{一定条件}{→}$
+n HO-CH2CH2-OH$\stackrel{一定条件}{→}$ +(2n-1)H2O
+(2n-1)H2O 、
、 .
.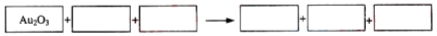

 与氧化剂物质的量之比为__________。
与氧化剂物质的量之比为__________。