题目内容
16.下列离子方程式中正确的是( )| A. | NH4HSO4溶液中加入少量NaOH稀溶液:NH4++OH-=NH3•H2O | |
| B. | Ca(ClO)2溶液中通入过量的二氧化硫气体:ClO-+SO2+H2O=HClO+HSO3- | |
| C. | 酸性高锰酸钾溶液中滴入少量过氧化氢:2MnO4-+7H2O2+6H+=2Mn2++6O2↑+10H2O | |
| D. | 为缓解胃酸过多,服含NaHCO3的抗酸药:HCO3-+H+=H2O+CO2↑ |
分析 A.氢氧化钠少量,氢离子优先与氢氧根离子反应;
B.次氯酸具有强氧化性,能够将亚硫酸氢根离子氧化成硫酸根离子;
C.根据电子守恒分析,该反应中违反了电子守恒;
D.碳酸氢根离子在离子方程式中需要保留整体.
解答 解:A.氢氧化钠不足,硫酸氢铵电离出的氢离子优先反应,正确的离子方程式为:H++OH-=H2O,故A错误;
B.二者发生氧化还原反应,正确的离子方程式为:Ca2++2ClO-+2H2O+2SO2═CaSO4↓+SO42-+4H++2Cl-,故B错误;
C.酸性高锰酸钾溶液中滴入少量过氧化氢,双氧水中氧元素被氧化成氧气,正确的离子方程式为:2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O,故C错误;
D.为缓解胃酸过多,服含NaHCO3的抗酸药,反应的离子方程式为:HCO3-+H+=H2O+CO2↑,故D正确;
故选D.
点评 本题考查了离子方程式的判断,题目难度中等,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.

练习册系列答案
相关题目
6.某无色透明溶液能与铝粉反应放出H2,则此溶液中可能存在( )
| A. | OH-、Ba2+、Cl-、Na+ | B. | H+、Cl-、Na+、SO${\;}_{4}^{2-}$ | ||
| C. | H+、Cu2+、[Al(OH)4]-、SO${\;}_{4}^{2-}$ | D. | H+、Ba2+、Mg2+、NO${\;}_{3}^{-}$ |
4.下列有关铁及其化合物的离子方程式一定错误的是( )
| A. | 铁与稀硝酸反应:Fe+4H++NO3-=Fe3++NO↑+2H2O | |
| B. | 磁性氧化铁与浓盐酸反应:Fe3O4+8H+=Fe2++2Fe3++4H2O | |
| C. | 氢氧化铁与氢碘酸反应:Fe(OH)3+3H+=Fe3++3H2O | |
| D. | 溴化亚铁溶液与足量氯水反应:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |
11.下列叙述不正确的是( )
| A. | 与28gCO具有相同分子数的CO2的质量一定是44g | |
| B. | 在标准状况下,11.2L某气体的质量为22g,则该气体的相对分子质量是44g/mol | |
| C. | 16gO2和16gO3含的氧原子个数一样多 | |
| D. | 1L1mol•L-1Fe(OH)3胶体中胶体微粒数目等于NA |
5.对于反应3S+6KOH=K2SO3+2K2S+3H2O的分析正确的是( )
| A. | S做还原剂 | B. | KOH做氧化剂 | C. | K2SO3做氧化剂 | D. | K2S做还原剂 |
6.下列说法正确的是( )
| A. | 维生素E 属于脂溶性维生素 | B. | 植物油的熔点比动物油高 | ||
| C. | 纤维素在人体内可以转化为脂肪 | D. | 脂肪是提供人体能量的主要的物质 |
 如果烧杯中最初装入的是500mL 2mol•L-1的稀硫酸溶液,构成铜锌原电池(见图,假设产生的气体没有损失),当在标准状况下收集到11.2L的氢气时,则此时烧杯内溶液中溶质的物质的量浓度分别为(溶液体积变化忽略不计)c(H2SO4)=1mol•L-1,c(ZnSO4)=1mol•L-1.
如果烧杯中最初装入的是500mL 2mol•L-1的稀硫酸溶液,构成铜锌原电池(见图,假设产生的气体没有损失),当在标准状况下收集到11.2L的氢气时,则此时烧杯内溶液中溶质的物质的量浓度分别为(溶液体积变化忽略不计)c(H2SO4)=1mol•L-1,c(ZnSO4)=1mol•L-1.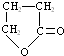 ,化合物C的结构简式是HOCH2CH=CHCOONa.
,化合物C的结构简式是HOCH2CH=CHCOONa. .
.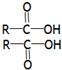 $→_{△}^{浓H_{2}SO4}$
$→_{△}^{浓H_{2}SO4}$


 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +H2O
+H2O
 +4NaOH$\stackrel{△}{→}$
+4NaOH$\stackrel{△}{→}$ +CH3COONa+4H2O+4CH3CH2CH2CH2OH.
+CH3COONa+4H2O+4CH3CH2CH2CH2OH.