题目内容
加碘盐的主要成分是NaCl,还添加了适量的KIO3。下列说法中正确的是
| A.KIO3和NaCl为离子化合物,均只含离子键 |
B.KIO3中阳离子的结构示意图为 |
| C.23Na37Cl中质子数和中子数之比是8∶7 |
| D.次碘酸的结构式为H—O—I |
D
解析试题分析:氯酸钾中还含有共价键,A不正确;氯酸钾中阳离子是K+,最外层电子数是8个,选项B不正确;23Na37Cl中质子数和中子数之比是(11+17):(12+20)=7∶8,C不正确;次碘酸中碘元素的化合价是+1价,氧元素是-2价,氢元素是+1价,因此结构式是H—O—I,选项D正确,答案选D。
考点:考查常见化学用语的正误判断
点评:该题是中等难度的试题,也是高考中的常见题型与重要的考点。该题基础性强,难易适中,主要是考查学生对常见化学用语的熟悉掌握程度。该类试题需要明确的是常见的化学用语主要包括元素符号、化学式、化合价、电子式、原子结构示意图、结构式、结构简式以及方程式和各种模型等,需要学生熟练记住,并能灵活运用。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
设NA为阿伏加德罗常数的数值,下列说法正确的是
| A.标准状况下,11.2 L CH3OH中含有C-H键1.5NA |
| B.9g18 8O2中含有的中子数为5NA |
| C.1 L pH=1的硫酸溶液中含有的H+数为0.2NA |
| D.1 mol Cu与足量S完全反应生成Cu2S,转移电子数为2NA |
下列化学用语表示正确的是 ( )
| A.HClO的结构式:H—O—Cl |
B.四氯化碳的电子式: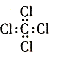 |
C.CO2的比例模型: |
| D.乙烯的结构简式:CH2CH2 |
已知25%的氨水的密度为0.91 g/ml,5%的氨水密度为0.98 g/ml,若将上述两种氨水等体积混合,所得氨水的质量分数 ( )
| A.等于15% | B.大于15% | C.小于15% | D.无法确定 |
用浓硫酸配制一定物质的量浓度的硫酸溶液,下列操作会造成所配溶液浓度偏高的是( )
| A.溶解后的溶液未冷却至室温就转移入容量瓶中 |
| B.反复倒转摇匀后,液面低于刻度线,再加蒸馏水至液面最低点恰好与刻度线相平 |
| C.洗涤烧杯和玻璃棒的溶液转移入容量瓶中 |
| D.定容时,眼睛仰视刻度线 |
在MgCl2、Cl2、Ca(ClO)2、HClO2、( )、Cl2O7的排列中,括号内应填入的物质的化学式是
| A.Cl2O3 | B.KClO4 | C.KClO3 | D.HClO |
铁、铝各1mol组成的混合物溶于一定量的盐酸,恰好完全反应后,再加入3mol Na2O2固体使之充分反应,最终产物是( )
| A.Fe(OH)2、Al(OH)3、NaCl |
| B.Fe(OH)2、Al(OH)3、NaAlO2、NaCl |
| C.Fe(OH)3、NaAlO2、NaCl |
| D.Fe(OH)3、Al(OH)3、NaAlO2、NaCl |