题目内容
已知下列热化学方程式:
Zn(s) + 1/2 O2(g)= ZnO(s) ΔH= -351.1 kJ·mol-1
Hg(l) + 1/2 O2(g)= HgO(s) ΔH= -90.7 kJ·mol-1
由此可![]() 知Zn(s)+ Hg
知Zn(s)+ Hg![]() O(s)= ZnO(s)+ Hg(l)的反应热ΔH为
O(s)= ZnO(s)+ Hg(l)的反应热ΔH为
A.-260.4 kJ·mol-1 B.+260.4 kJ·mol-1 C.- 441.8 kJ·mol-1 D.+ 4![]() 41.8 kJ·mol-1
41.8 kJ·mol-1
A
解析:
根据盖斯定律有:△H= -351.1 kJ·mol-1-(-90.7 kJ·mol-1 )=-260.4kJ·mol-1。

练习册系列答案
相关题目
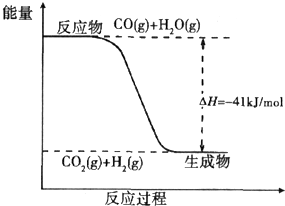 煤炭可以转化为清洁能源和化工原料.
煤炭可以转化为清洁能源和化工原料.