题目内容
将浓度为0.2mol?L-1NH4Cl溶液加水不断稀释,下列各量增大的是( )
| A、c(H+) | ||
| B、Kh(NH4Cl)(水解常数) | ||
| C、c(OH-) | ||
D、c(NH
|
考点:盐类水解的应用
专题:盐类的水解专题
分析:加水稀释促进氯化铵水解,但溶液中氢离子浓度减小导致溶液的酸性减弱,温度不变,水的离子积常数、盐类水解平衡常数都不变,据此分析解答.
解答:
解:A.加水稀释促进铵根离子水解,但铵根离子水解增大程度小于溶液体积增大程度,所以c(H+)减小,故A错误;
B.水解平衡常数只与温度有关,温度不变,则氯化铵水解平衡常数不变,故B错误;
C.加水稀释导致溶液中氢离子浓度减小,温度不变,水的离子积常数不变,则c(OH-)增大,故C正确;
D.加水稀释促进铵根离子水解,溶液体积增大,所以铵根离子浓度降低,故D错误;
故选C.
B.水解平衡常数只与温度有关,温度不变,则氯化铵水解平衡常数不变,故B错误;
C.加水稀释导致溶液中氢离子浓度减小,温度不变,水的离子积常数不变,则c(OH-)增大,故C正确;
D.加水稀释促进铵根离子水解,溶液体积增大,所以铵根离子浓度降低,故D错误;
故选C.
点评:本题考查了盐类水解,明确盐类水解特点是解本题关键,知道影响电离平衡常数及离子积平衡常数的因素,题目难度不大.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案
相关题目
下列各有机物的命名中正确的是( )
| A、CH3-CH═CH-CH3 二丁烯 |
| B、CH3OOCC2H5 乙酸乙酯 |
C、 2-甲基-3-丁醇 2-甲基-3-丁醇 |
D、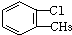 邻氯甲苯 邻氯甲苯 |
下列离子反应方程式正确的是( )
| A、次氯酸钙溶液中通入少量二氧化碳:Ca2++2ClO-+H2O+CO2═CaCO3↓+2H++2ClO- |
| B、澄清的石灰水跟盐酸反应:H++OH-=H2O |
| C、碳酸氢钠溶液中滴入氢氧化钙溶液:HCO3-+OH-═CO32-+H2O |
| D、硫化钡中加入足量稀硫酸:BaS+2H+═H2S↑+Ba2+ |
下列过程中,共价键被破坏的是( )
| A、HCl气体溶于水 |
| B、NaCl固体溶于水 |
| C、酒精溶于水 |
| D、碘升华 |
下列说法正确的是( )
| A、聚乙烯能使溴水褪色 |
| B、油脂是天然高分子化合物 |
| C、淀粉和纤维素都是高分子化合物而且分子式相同 |
| D、生成高分子化合物的常见反应是加聚反应和缩聚反应 |
下列两种气体所含微粒数一定相等的是( )
| A、等温等体积的O2和N2中的原子数 |
| B、等体积等密度的NO和C2H4中的分子数 |
| C、等温等质量的S2和S4中的原子数 |
| D、等压等体积的N2和CO2中的分子数 |
下列有关氯气的说法正确的是( )
| A、氯气是黄绿色气体,有毒,有刺激性气味,不能溶于水 |
| B、将氯气持续通入紫色石蕊试液中先变红后褪色 |
| C、红热的铜丝在Cl2中燃烧产生棕黄色的雾 |
| D、氯水长时间放置不会变质,还可消毒杀菌 |
