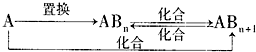题目内容
图中X、Y、Z、 W是地壳含量前四位(不按顺序)的元素组成的单质,其它为化合物,A有磁性。它们之间存在如下转化关系(部分产物已略去)。

回答下列问题:
(1)组成单质Y的元素在周期表中的位置是 , M的化学式是 ;
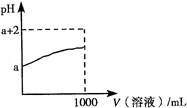
(2)胶体的应用非常广泛,早在150年前的1862年,英国科学家格雷阿姆就提出了"胶体"的概念,R胶体中分散质直径大小范围为: ,可利用 区分胶体和溶液;
(3)写出A与 W反应的化学方程式: ;
(4)写出A和足量D的稀溶液反应生成G的离子方程式:
(5)简述检验G溶液中的金属阳离子的实验方法(操作、现象、结论)
(6)工业由E制备Z的反应方程式
(1)第二周期第ⅥA族,Na2SiO3;
(2)1 nm~100 nm 丁达尔效应;
(3)8Al+3Fe3O4=9Fe+4Al2O3
(4)3Fe3O4+28H++NO3-=9Fe3++NO↑+14H2O
(5)取少量Fe(NO3)3溶液于一支试管中,加入几滴KSCN溶液,溶液呈血红色,证明含Fe3+ (其它合理答案也给分)
(6)SiO2 + 2C = Si + 2CO↑ (3、6问条件为注明应为“高温”)

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示.若Y原子的最外层电子数是次外层电子数的3倍,下列说法正确的是( )
| X | Y | |
| Z | W |
| A、原子半径:W>Z>Y>X |
| B、最高价氧化物对应水化物的酸性:Z>W>X |
| C、4种元素的氢化物中,Z的氢化物最稳定 |
| D、X的最高价氧化物对应的水化物能与其气态氢化物发生反应 |
 五种短周期元素X、Y、Z、W、Q(X、Y、Z、W、Q分别代表元素符号)在周期表中的位置如右图所示.下列说法中,不正确的是( )
五种短周期元素X、Y、Z、W、Q(X、Y、Z、W、Q分别代表元素符号)在周期表中的位置如右图所示.下列说法中,不正确的是( )| A、X的气态氢化物与Q的气态氢化物相遇会产生白烟 | B、元素的非金属性:Y>Q,同浓度的氢化物水溶液的酸性:HY<HQ | C、形成简单离子的半径从小到大的顺序是:Y-<Q-<W2- | D、Z的最高价氧化物可溶于水,也能溶于强碱溶液 |
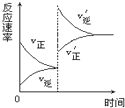 对达到平衡状态的可逆反应X+Y?Z+W,在其他条件不变的情况下,增大压强,反应速率变化如图所示,则图象中关于X、Y、Z、W四种物质的聚集状态为( )
对达到平衡状态的可逆反应X+Y?Z+W,在其他条件不变的情况下,增大压强,反应速率变化如图所示,则图象中关于X、Y、Z、W四种物质的聚集状态为( )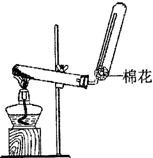 (2010?崇文区二模)X、Y、Z、W均为含有10电子的微粒,其中X、Y、Z为分子,W为离子,且X与Z分子中含有的共用电子对数之比为3:4.
(2010?崇文区二模)X、Y、Z、W均为含有10电子的微粒,其中X、Y、Z为分子,W为离子,且X与Z分子中含有的共用电子对数之比为3:4.