题目内容
(本题共14分)A、B、D、E、F为短周期元素,元素A最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍。B 在D中充分燃烧能生成其最高价化合物BD2。E+与D2-具有相同的电子数。A在F中燃烧,产物溶于水得到一种强酸。回答下列问题:
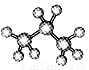
(1)D在周期表中的位置是 ,A与B组成的一种化合物中A的质量分数为25%,则该化合物的空间构型 ,A2D的沸点高于BD2的原因 ;
(2)比较B、D、E的原子半径 (用元素符号表示);
(3)上述五种元素间可形成多种化合物,写出含有元素A的二元离子化合物与A2D反应的化学方程式 ;
(4)写出一种工业制备单质F的离子方程式 ;
(5)由D与E组成的既含离子键又含共价键的化合物与BD2反应的化学方程式 ;
(6)B、E、 D组成一种水溶液呈碱性的盐,其原子个数之比为1 :2 :3 ,请设计一个简单的实验检验该盐的化学成份。 。
(1)第二周期第VIA族(1分) ,正四面体(1分) ,水中存在氢键(2分)
(2)rO<rC <rNa (2分) (3)NaH+H2O=NaOH+H2 ↑ (2分)
(4)2Cl-+2H2O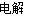 2OH-+H2↑+Cl2↑(2分) (5)2Na2O2+2CO2=2Na2CO3+O2 (2分)
2OH-+H2↑+Cl2↑(2分) (5)2Na2O2+2CO2=2Na2CO3+O2 (2分)
(6)取少量固体样品于试管中加蒸馏水将其溶解,取少量溶液于另一试管中,加少量稀盐酸,将产生的无色无味气体通入到澄清的石灰水中,若澄清的石灰水变浑浊,证明溶液中含有CO32- ,再用洁净的铂丝蘸取原样品溶液放在酒精灯上灼烧,若观察到黄色火焰,证明溶液中含有Na+ ,所以该盐为Na2CO3(2分)
【解析】
试题分析:A,B,D,E,F为短周期元素,非金属元素A最外层电子数与其周期数相同,则A为H;B的最外层电子数是其所在周期数的2倍,则B为C或S,B在D中充分燃烧能生成其最高价化合物BD2,则D为O,B的最高正价为+4价,则B为C;E+与D2-具有相同的电子数,则E为Na;A在F中燃烧,产物溶于水得到种强酸,则F为Cl,则
(1)氧元素的原子序数是8,在周期表中的位置是第二周期第VIA族;A与B组成的一种化合物中A的质量分数为25%,则该化合物是甲烷,其分子的空间构型正四面体;水分子间存在氢键,所以水的沸点高于CO2的沸点;
(2)同周期自左向右原子半径逐渐减小,同主族自上而下原子半径逐渐增大,则较B、D、E的原子半径大小顺序是;rO<rC <rNa;
(3)元素A的二元离子化合物与水反应,因此该化合物是NaH,反应的化学方程式为NaH+H2O=NaOH+H2 ↑;
(4)工业上常用电解饱和食盐水的方法来制备氯气,其电解离子方程式为:2Cl-+2H2O 2OH-+H2↑+Cl2↑;
2OH-+H2↑+Cl2↑;
(5)由D与E组成的既含离子键又含共价键的化合物是过氧化钠,与BD2反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2;
(6)B、E、 D组成一种水溶液呈碱性的盐,其原子个数之比为1 :2 :3 ,因此该化合物是碳酸钠。碳酸根可以用盐酸、澄清石灰水检验,钠离子用焰色反应检验,即取少量固体样品于试管中加蒸馏水将其溶解,取少量溶液于另一试管中,加少量稀盐酸,将产生的无色无味气体通入到澄清的石灰水中,若澄清的石灰水变浑浊,证明溶液中含有CO32- ,再用洁净的铂丝蘸取原样品溶液放在酒精灯上灼烧,若观察到黄色火焰,证明溶液中含有Na+ ,所以该盐为Na2CO3。
考点:考查元素推断的有关判断与应用

 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案下列关于离子共存的评价及离子方程式书写正确的是
选项 | 离子组 | 评价 |
A | H+、Mg2+、Br-、NO3- | 能大量共存于同一溶液中,投入少量锌粉后,可放出H2 ,反应的离子方程式为 Zn+ 2H+ = Zn2++ H2↑ |
B | NH4+、CO32-、Cl-、Al3+ | 不能大量共存于同一溶液中,因为有沉淀生成 2Al3++3CO32-=Al2(CO3)3↓ |
C | ClO-、Na+、K+、HSO3- | 能大量共存于同一溶液中 |
D | HCO3-、OH-、Na+、K+ | 不能大量共存于同一溶液中,因为发生如下反应 HCO3-+ OH-= CO32-+ H2O |
奥运会会标是五环旗,假定奥运五环旗中的一环表示一种物质,相连环物质间一定条件下能发生常见反应,不相连环物质间不能发生反应,且四种反应中必须包含化合反应、置换反应及复分解反应,适合的一组是 ( )
| 蓝 | 黄 | 黑 | 绿 | 红 |
A | SiO2 | NaOH溶液 | CuSO4溶液 | Ag | O2 |
B | O2 | Fe | 稀H2SO4 | NaOH溶液 | CO2 |
C | O2 | NH3 | 稀H2SO4 | NaOH溶液 | Al(OH)3 |
D | Mg | Al | CO2 | Fe2O3 | KOH溶液 |
 乙
乙 丙
丙 甲,则甲不可能是
甲,则甲不可能是 n Z (g) △H > 0,将X和Y以一定比例混合通入密闭容器中进行反应,各物质的浓度随时间的改变如图所示。下列说法不正确的是( )
n Z (g) △H > 0,将X和Y以一定比例混合通入密闭容器中进行反应,各物质的浓度随时间的改变如图所示。下列说法不正确的是( )
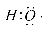 组成元素相同,含有的电子数也相同
组成元素相同,含有的电子数也相同