题目内容
一定条件下,某容积为1L的密闭容器中发生如下反应:
C(s)+H2O(g) CO(g)+H2 (g)
CO(g)+H2 (g)
(1)维持温度不变,向该容器中充入2 mol C(s)和2 mol H2O(g),达到平衡后混合气体的平均相对分子质量为Mr,则Mr的范围为 。
(2)达到平衡后,保持容器容积不变,向体系中再加入一定质量的C,逆反应速率 (填“增大”、 “减小”或“不变”),化学平衡 (填“正移”、 “逆移”或“不变”);若保持温度不变,压缩容积,逆反应速率 ,化学平衡 。
【答案】
(11分)
(1)15<Mr<18(3分)
(2)不变 不变 增大 逆移(8分)
【解析】
试题分析:
C(s) + H2O(g) CO(g) + H2
(g)
CO(g) + H2
(g)
起始浓度 2 mol 2 mol
极限值之一是当反应物完全转化成生成物时,即体系中只有 CO(g) 和 H2 (g)
混合气体的平均相对分子质量为Mr=m气体总/n气体总 =(2×18+2×12)/4 =15
极限值之二是当反应物完全不转化成生成物时,即体系中只有C(s)和 H2O(g)
混合气体的平均相对分子质量为Mr=MH2O =18;则Mr的范围为15<Mr<18;
达到平衡后,保持容器容积不变,向体系中再加入一定质量的C,逆反应速率 不变,化学平衡不变;若保持温度不变,压缩容积,逆反应速率增大,化学平衡逆向移动
考点:化学平衡的影响因素 极限法的应用
点评:此题要用到极限法求解。学生需要注意的是由于该反应是可逆反应,所以极限值达不到。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
一定条件下,某密闭容器中充入物质的量相等的A、B两种气体,发生反应:A(g)+B(g)?2C(g).达到平衡后,只改变反应的一个条件,测得容器中各物质的浓度、反应速率随时间变化如下两图所示.下列说法中正确的是( )
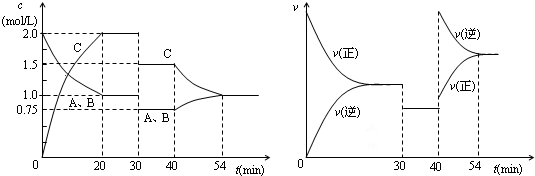

| A、30min时减小容积 | B、40min时加入催化剂 | C、正反应为吸热反应 | D、0~20min内 A的平均反应速率为0.05mol?L-1?min-1 |
 2NH3.在10s内N2的浓度由5mol/L降至4mol/L下列说法正确的是( )
2NH3.在10s内N2的浓度由5mol/L降至4mol/L下列说法正确的是( ) CH3OCH3(g)+3H2O(g);△H<0.
CH3OCH3(g)+3H2O(g);△H<0.
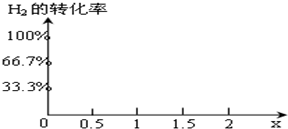
 CO(g)+H2 (g)
CO(g)+H2 (g)