题目内容
根据等电子原理,下列分子或离子与SO42-有相似结构的是( )
| A、PCl5 |
| B、CCl4 |
| C、NF3 |
| D、NO3- |
考点:判断简单分子或离子的构型
专题:原子组成与结构专题
分析:原子个数相等、价电子数相等的微粒互为等电子体,等电子体的结构相似,据此分析解答.
解答:
解:原子个数相等、价电子数相等的微粒互为等电子体,等电子体的结构相似,SO42-中原子个数是5、价电子数是32,
A.PCl5中原子个数是6、价电子数是40,所以与硫酸根离子不是等电子体,其结构不同,故A错误;
B.CCl4中原子个数是5、价电子数是32,所以与硫酸根离子是等电子体,其结构相似,故B正确;
C.NF3中原子个数是5、价电子数是26,所以与硫酸根离子不是等电子体,其结构不同,故C错误;
D.NO3-中原子个数是4、价电子数是24,所以与硫酸根离子不是等电子体,其结构不同,故D错误;
故选B.
A.PCl5中原子个数是6、价电子数是40,所以与硫酸根离子不是等电子体,其结构不同,故A错误;
B.CCl4中原子个数是5、价电子数是32,所以与硫酸根离子是等电子体,其结构相似,故B正确;
C.NF3中原子个数是5、价电子数是26,所以与硫酸根离子不是等电子体,其结构不同,故C错误;
D.NO3-中原子个数是4、价电子数是24,所以与硫酸根离子不是等电子体,其结构不同,故D错误;
故选B.
点评:本题以硫酸根离子为载体考查等电子体、微粒空间构型,侧重考查分析计算能力,知道等电子体概念及其性质,也可以根据价层电子对理论确定空间构型,题目难度不大.

练习册系列答案
 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
下列各组离子在溶液中能够大量共存的是( )
| A、NH4+、Ca2+、OH-、CO32- |
| B、NH4+、Br-、Na+、SO42- |
| C、Ag+、H+、SO32-、ClO- |
| D、H+、Cl-、Fe2+、NO3- |
下列用电子式表示的形成过程正确的是( )
A、H×+?Cl:→H+[
| ||||
B、Na×+?Br:→Na
| ||||
C、×Mg×+2?F:→Mg2+[
| ||||
D、 |
1866年凯库勒提出了苯的单、双键交替的正六边形平面结构,解释了苯的部分性质,但还有一些问题尚未解决,它不能解释下列事实( )
| A、苯不能使溴水褪色 |
| B、苯能与H2发生加成反应 |
| C、溴苯没有同分异构体 |
| D、苯能燃烧 |
下列叙述中正确的是( )
| A、所有的非金属元素都在p区 |
| B、P原子的价电子排布式为3s23p3 |
| C、过渡元素都在d区 |
| D、当各轨道处于全满、半满、全空时原子较稳定 |
下列物质:①乙烷;②苯;③聚乙烯;④聚氯乙烯;⑤丁炔;⑥环己烷;⑦邻二甲苯;⑧3-甲基-1-戊烯.其中能使酸性KMnO4溶液褪色,也能与溴水发生化学反应而褪色的是( )
| A、⑤⑧ | B、③⑤⑦⑧ |
| C、③④⑤⑦ | D、④⑤⑦ |
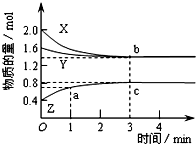 某温度时,在体积为2L的密闭容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如图所示,其中a、b、c三点的坐标分别为(1,0.7)、(3,1.4)、(3,0.8).下列说法中正确的是( )
某温度时,在体积为2L的密闭容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如图所示,其中a、b、c三点的坐标分别为(1,0.7)、(3,1.4)、(3,0.8).下列说法中正确的是( )| A、该反应的化学方程式是3X+Y=2Z |
| B、3 min时,X的转化率为70% |
| C、达平衡时,c(Y)=0.7 mol?L-1 |
| D、前1 min内,v(Z)=0.3 mol?L-1?min-1 |
用石墨电极电解足量硝酸银溶液,在阳极收集到0.40克氧气,中和电解时生成的酸需250 毫升氢氧化钠溶液,则氢氧化钠溶液的浓度是( )
| A、0.20 摩/升 |
| B、0.15 摩/升 |
| C、0.10 摩/升 |
| D、0.05 摩/升 |
