题目内容
3.aAm+和bBn-核外电子层结构相同,则a值为( )| A. | b+n-m | B. | b-m-n | C. | b+n+m | D. | b-n+m |
分析 aAm+和bBn-的核外电子排布相同,说明二者核外电子数相同,即a-m=b+n,由此分析解答.
解答 解:核外电子层结构相同即表示核外电子数相等,aAm+核外电子数等于质子数减去离子所带的电荷数,即(a-m),bBn-核外电子数等于质子数加上离子所带的电荷数,即(b+n),因此a-m=b+n,则a=b+n+m,
故选C.
点评 本题考查结构与位置关系,难度不大,确定元素的相对位置是解题关键.

练习册系列答案
相关题目
13.下图所示的实验方法、装置或操作中正确的是( )
| A. |  干燥SO2 | B. |  实验室制取并收集O2 | ||
| C. |  装置气密性的检查 | D. |  吸收氨气 |
18.草酸是一种重要的化工原料,广泛用于药物生产、高分子合成等工业.某学习小组的同学拟以甘蔗渣为原料用水解-氧化-水解循环进行制取草酸.查阅资料得知:
①易溶于乙醇和水,微溶于乙醚(易挥发),难溶于苯和四氯化碳.
②草酸具有很强的还原性

请跟据以上信息回答下列问题:
(1)氧化-水解过程是在上图1的装置中进行的,指出装置A的名称三颈烧瓶.
(2)氧化-水解过程中,在硝酸用量、反应的时间等条件均相同的情况下,改变反应温度以考察反应温度对草酸产率的影响,结果如图2所示,请选择最佳的反应温度为70℃,实验中若混酸滴加过快或温度过高,将导致草酸产率下降,其原因是草酸易被浓硫酸或硝酸氧化.
(3)得到粗产品后,洗涤时选择乙醚 作洗涤剂,理由是易挥发,无残留.
(4)为了确定产品中H2C2O4•2H2O(M=126g/mol)的纯度,称取10.0g草酸样品,配成250mL溶液,每次实验时准确量取25.00mL草酸溶液,加入适量的稀硫酸,用0.1mol/LKMnO4标准溶液滴定.平行滴定三次,重复滴定三次,每次消耗KMnO4标准溶液的体积如表所示
①写出滴定过程中的离子方程式5H2C2O4+2MnO4-+6H+=2Mn2++10CO2↑+8H2O.
②在草酸纯度测定的实验过程中,下列说法正确的是:CD.
A.配制标准液时,若KMnO4不纯(杂质不与待测液反应),会使实验误差偏低
B.润洗滴定管时,应从滴定管上口加满所需的酸或碱液,使滴定管内壁充分润洗
C.滴定时,眼睛注视锥形瓶,观察溶液颜色变化
D.滴定终点读取滴定管刻度时,仰视标准液液面,会使实验误差偏高
③判断滴定已经达到终点的方法是:锥形瓶中滴入最后一滴高锰酸钾标准液,锥形瓶中溶液变成浅红色且半分钟后不变色.
④草酸晶体的纯度为50.4%.
①易溶于乙醇和水,微溶于乙醚(易挥发),难溶于苯和四氯化碳.
②草酸具有很强的还原性

请跟据以上信息回答下列问题:
(1)氧化-水解过程是在上图1的装置中进行的,指出装置A的名称三颈烧瓶.
(2)氧化-水解过程中,在硝酸用量、反应的时间等条件均相同的情况下,改变反应温度以考察反应温度对草酸产率的影响,结果如图2所示,请选择最佳的反应温度为70℃,实验中若混酸滴加过快或温度过高,将导致草酸产率下降,其原因是草酸易被浓硫酸或硝酸氧化.
(3)得到粗产品后,洗涤时选择乙醚 作洗涤剂,理由是易挥发,无残留.
(4)为了确定产品中H2C2O4•2H2O(M=126g/mol)的纯度,称取10.0g草酸样品,配成250mL溶液,每次实验时准确量取25.00mL草酸溶液,加入适量的稀硫酸,用0.1mol/LKMnO4标准溶液滴定.平行滴定三次,重复滴定三次,每次消耗KMnO4标准溶液的体积如表所示
| 第一次 | 第二次 | 第三次 | |
| 体积(mL) | 16.10mL | 16.60mL | 15.90mL |
②在草酸纯度测定的实验过程中,下列说法正确的是:CD.
A.配制标准液时,若KMnO4不纯(杂质不与待测液反应),会使实验误差偏低
B.润洗滴定管时,应从滴定管上口加满所需的酸或碱液,使滴定管内壁充分润洗
C.滴定时,眼睛注视锥形瓶,观察溶液颜色变化
D.滴定终点读取滴定管刻度时,仰视标准液液面,会使实验误差偏高
③判断滴定已经达到终点的方法是:锥形瓶中滴入最后一滴高锰酸钾标准液,锥形瓶中溶液变成浅红色且半分钟后不变色.
④草酸晶体的纯度为50.4%.
15.下列各组离子中,能在水溶液中大量共存,且溶液显酸性的是( )
①Na+、H+、SO42-、HCO3-
②K+、Al3+、H2PO4-、HCO3-
③Na+、H+、Cl-、C6H5O-
④H+、Fe2+、NO3-、Cl-
⑤Na+、Al3+、NO3-、AlO2-
⑥Cu2+、Mg2+、SO42-、NO3-.
①Na+、H+、SO42-、HCO3-
②K+、Al3+、H2PO4-、HCO3-
③Na+、H+、Cl-、C6H5O-
④H+、Fe2+、NO3-、Cl-
⑤Na+、Al3+、NO3-、AlO2-
⑥Cu2+、Mg2+、SO42-、NO3-.
| A. | ②③⑤ | B. | ①⑥ | C. | ①④⑤ | D. | 只有⑥ |
12.下列关于物质物分类的说法正确的组合是( )
①非金属氧化物一定是酸性氧化物
②金属氧化物不一定是碱性氧化物
③碱性氧化物一定是金属氧化物
④Na2O和Na2O2均能与H2O反应生成NaOH,故二者都是碱性氧化物
⑤纯净物是由一种元素组成,而混合物由两种或两种以上元素组成
⑥只由一种元素的阳离子与另一种元素的阴离子组成的物质一定为纯净物.
①非金属氧化物一定是酸性氧化物
②金属氧化物不一定是碱性氧化物
③碱性氧化物一定是金属氧化物
④Na2O和Na2O2均能与H2O反应生成NaOH,故二者都是碱性氧化物
⑤纯净物是由一种元素组成,而混合物由两种或两种以上元素组成
⑥只由一种元素的阳离子与另一种元素的阴离子组成的物质一定为纯净物.
| A. | ①④⑤⑥ | B. | ②③ | C. | ③④⑥ | D. | ②③⑥ |
13.相同温度、相同浓度的下列电解质溶液,其pH由小到大的顺序如图所示,图中①②③代表的物质可能分别是( )
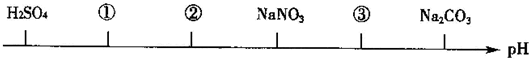
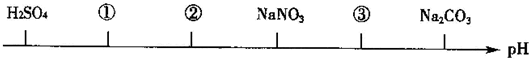
| A. | CuCl2 CH3COOH NaOH | B. | HCl H2SO3 NaHCO3 | ||
| C. | HF HCl CH3COONa | D. | NH4Cl HCl CH3COONa |


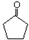 ,G中官能团的名称为碳碳双键、酯基.
,G中官能团的名称为碳碳双键、酯基. ,反应类型加成反应.
,反应类型加成反应. 病人输液用的葡萄糖注射液是葡萄糖(C6H12O6)的水溶液,其标签上的部分内容如图所示.利用标签所提供的信息,回答下列问题:
病人输液用的葡萄糖注射液是葡萄糖(C6H12O6)的水溶液,其标签上的部分内容如图所示.利用标签所提供的信息,回答下列问题: