题目内容
相同温度下,两种氨水A、B,浓度分别是0.2mol/L和0.1mol/L,则A和B的OH-浓度之比( )
| A、大于2 | B、小于2 |
| C、等于2 | D、不能确定 |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:弱电解质溶液中,弱电解质的浓度越大,其电离程度越小,浓度越小,其电离程度越大.
解答:
解:一水合氨是弱电解质,在溶液里存在电离平衡,氨水的浓度越大,一水合氨的电离程度越小,浓度越小,一水合氨的电离程度越大,
A瓶氨水的浓度是B瓶氨水的浓度的2倍,因弱电解质的浓度越小,电离程度越大,故A瓶氨水的电离度比B瓶氨水的电离度小,
所以A、B两瓶氨水中[OH-]之比小于2,
故选:B.
A瓶氨水的浓度是B瓶氨水的浓度的2倍,因弱电解质的浓度越小,电离程度越大,故A瓶氨水的电离度比B瓶氨水的电离度小,
所以A、B两瓶氨水中[OH-]之比小于2,
故选:B.
点评:本题考查弱电解质的电离程度与浓度的关系,明确一水合氨的电离程度是解答本题的关键.

练习册系列答案
相关题目
用下列实验装置进行相应实验,能达到实验目的是( )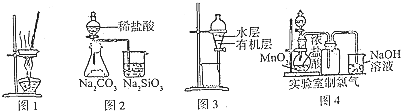

| A、用图l所示装置蒸干AlC13饱和溶液制备AlCl3晶体 |
| B、用图2所示装置证明非金属性Cl>C>Si |
| C、用图3所示装置分离CCl4萃取溴水后已分层的有机层和水层 |
| D、用图4所示装置制取少量Cl2气体 |
用铂作电极电解某金属氯化物MCln的水溶液,当阳极产生a mol气体时,阴极析出m g金属(无气体生成),则金属的相对原子质量是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
汽车尾气中的污染物除碳氢化合物、可吸入颗粒物、一氧化碳外,还主要含有( )
| A、氮氧化物 | B、氮气 |
| C、水蒸气 | D、氧气 |
下列各组离子中,在酸性溶液中能大量共存的离子组是( )
| A、Na+、MnO4-、Mg2+、NO3- |
| B、Na+、Ba2+、SO42-、Br- |
| C、K+、SCN-、Fe3+、Cl- |
| D、K+、AlO2-、Cl-、SO42- |
下列过程属于物理变化的是( )
| A、煤的气化 | B、石油分馏 |
| C、石油裂解 | D、煤的直接液化 |
将少量的CO2通入下列溶液中,没有沉淀产生的是( )
| A、Ba(OH)2溶液 |
| B、澄清石灰水 |
| C、氯化钡溶液 |
| D、漂白粉溶液 |
在pH=1的溶液中,能大量共存的一组离子是( )
| A、Mg2+、Ca2+、HCO3-、NO3- |
| B、Al3+、NH4+、Br-、Cl- |
| C、K+、MnO4-、S2-、SO42- |
| D、Na+、K+、SiO32-、Cl- |