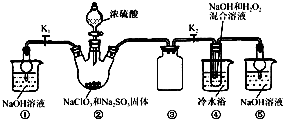
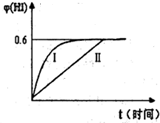
题目内容
已知反应
试回答下列问题:
(1)两次操作过程中指针为什么会发生偏转?________________________________________。
(2)两次操作过程中指针偏转方向为什么相反?试用化学平衡移动原理解释。____________________________。
(3)①操作过程中C1棒上发生的反应为______________________________________________。
(4)②操作过程中C2棒上发生的反应为______________________________________________。
(1)该实验条件下化学能转化为电能
(2)由于氢离子浓度的改变,使化学平衡向不同方向移动,因而发生了不同方向的反应
(3)2I--2e-![]() I2
I2
(4)![]() +H2O-2e-
+H2O-2e-![]()
![]() +2H+
+2H+
解析:![]() +2I-+2H+
+2I-+2H+![]()
![]() +I2+H2O是可逆反应,平衡移动方向受c(H+)影响。加入HCl,平衡正向移动,加入NaOH平衡逆向移动。两次原电池反应发生的方向相反,电流表指针相反。
+I2+H2O是可逆反应,平衡移动方向受c(H+)影响。加入HCl,平衡正向移动,加入NaOH平衡逆向移动。两次原电池反应发生的方向相反,电流表指针相反。
加HCl时,负极的电极反应为2I--2e-![]() I2
I2
正极的电极反应为![]() +2H++2e-
+2H++2e-![]()
![]() +H2O
+H2O
加NaOH时,负极的电极反应为![]() +H2O-2e-
+H2O-2e-![]()
![]() +2H+
+2H+
正极的电极反应为I2+2e-![]() 2I-
2I-

练习册系列答案
相关题目