题目内容
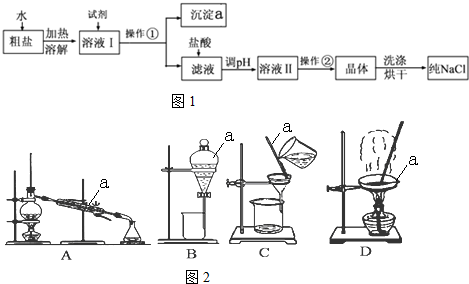
8.下列叙述正确的是( )| A. | 用苯萃取碘水中的碘,后分液,水层从上口倒出 | |
| B. | 金属氧化物都是碱性氧化物 | |
| C. | 三氯化铁溶液滴入氢氧化钠溶液可制备氢氧化铁胶体 | |
| D. | 可用量筒准确量取9.5ml水 |
分析 A.分液时下层液体从下口流出,避免重新混合而污染;
B.氧化铝为两性氧化物;
C.易生成氢氧化铁沉淀;
D.量筒精确到0.1mL.
解答 解:A.水的密度比苯大,分液时下层液体从下口流出,避免重新混合而污染,则水从下口流出,故A错误;
B.金属氧化物不一定为碱性氧化物,如氧化铝为两性氧化物,故B错误;
C.三氯化铁溶液滴入氢氧化钠溶液易生成氢氧化铁沉淀,应用水解的方法制备,故C错误;
D.量筒精确到0.1mL,可量取9.5ml水,故D正确.
故选D.
点评 本题考查化学实验方案的评价,为高频考点,涉及混合物分离提纯、胶体的制备以及量筒的使用等实验操作,把握混合物分离实验基本操作为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
18.在容积一定的密闭容器中,反应2A?B (g)+C (g)达到平衡后,升高温度容器内气体密度增大,则下列叙述正确的是( )
| A. | 改变压强对该平衡的移动无影响 | |
| B. | 正反应是放热反应且A不是气态 | |
| C. | 其它条件不变,加入少量A,该平衡向正反应方向移动 | |
| D. | 正反应是吸热反应且A不是气态 |
16.某混合溶液中溶质所含离子的物质的量浓度如表,则下列有关说法不正确的是( )
| 溶质所含离子 | SO42- | M | Mg2+ | Fe2+ |
| 物质的量浓度 | c | 3 | 3 | 2 |
| A. | 若M是NO3-,则c为3.5 | |
| B. | 若使Fe2+浓度降低,可以加入试剂NaOH | |
| C. | 若M是NH4+,则配制溶液所用的溶质不一定是3种 | |
| D. | 若加入BaCl2溶液能产生两种沉淀,则M可能是CO32- |
3.下列分子式表示的物质一定是纯净物的是( )
| A. | C2H6O | B. | C2H4Cl2 | C. | CH4O | D. | C |
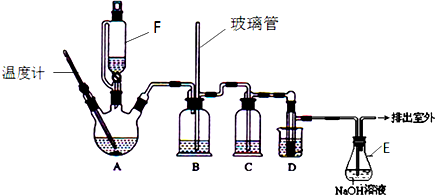
7.1,2-二溴乙烷可作汽油抗爆剂的添加剂,在实验室中可以用下图所示装置制备1,2-二溴乙烷.其中A和F中装有乙醇和浓硫酸的混合液,D中的试管里装有液溴.可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.(夹持装置已略去)
有关数据列表如下:
填写下列空白:
(1)A中主要发生的是乙醇的脱水反应,即消去反应,请你写出乙醇的这个消去反应的化学方程式:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O.D中发生反应的化学方程式为:CH2=CH2+Br2→CH2BrCH2Br.
(2)安全瓶B可以防止倒吸,并可以检查实验进行时导管是否发生堵塞.请写出发生堵塞时瓶B中的现象.b中水面会下降,玻璃管中的水柱会上升,甚至溢出
(3)在装置C中应加入c,其目的是吸收反应中可能生成的酸性气体:(填正确选项前的字母)a.水 b.浓硫酸c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(4)容器E中NaOH溶液的作用是吸收挥发出来的溴,防止污染环境.
(5)若产物中有少量副产物乙醚.可用蒸馏(填操作名称)的方法除去.
(6)反应过程中应用冷水冷却装置D,其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是1,2-二溴乙烷的凝固点较低(9℃),过度冷却会使其凝固而使导管堵塞.

有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | 一l30 | 9 | -1l6 |
(1)A中主要发生的是乙醇的脱水反应,即消去反应,请你写出乙醇的这个消去反应的化学方程式:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O.D中发生反应的化学方程式为:CH2=CH2+Br2→CH2BrCH2Br.
(2)安全瓶B可以防止倒吸,并可以检查实验进行时导管是否发生堵塞.请写出发生堵塞时瓶B中的现象.b中水面会下降,玻璃管中的水柱会上升,甚至溢出
(3)在装置C中应加入c,其目的是吸收反应中可能生成的酸性气体:(填正确选项前的字母)a.水 b.浓硫酸c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(4)容器E中NaOH溶液的作用是吸收挥发出来的溴,防止污染环境.
(5)若产物中有少量副产物乙醚.可用蒸馏(填操作名称)的方法除去.
(6)反应过程中应用冷水冷却装置D,其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是1,2-二溴乙烷的凝固点较低(9℃),过度冷却会使其凝固而使导管堵塞.