题目内容
17.下列用水就能鉴别的一组物质是( )| A. | 苯、己烷、四氯化碳 | B. | 苯、酒精、四氯化碳 | ||
| C. | 溴苯、酒精、四氯化碳 | D. | 硝基苯、酒精、醋酸 |
分析 水就能鉴别的一组物质,与水的溶解性不同、与水的密度不同,产生不同现象则可以鉴别,以此来解答.
解答 解:A.苯、己烷、四氯化碳都不溶于水,但苯和己烷的密度都小于水,无法鉴别,故A错误;
B.苯和四氯化碳都不溶于水,但苯的密度比水小,四氯化碳的密度比水大,乙醇与水混溶,可鉴别,故B正确;
C.溴苯、四氯化碳都不溶于水,且密度均比水的大,无法鉴别,故C错误;
D.酒精、醋酸都溶于水,不能鉴别,故D错误.
故选B.
点评 本题考查有机物的鉴别,为高频考点,侧重于学生的分析能力的考查,题目难度不大,注意把握常见有机物的性质,学习中要加强基础知识的积累,明确密度、溶解性即可解答.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.蛇纹石矿可看作由MgO、Fe2O3、Al2O3、SiO2组成.由蛇纹石制碱式碳酸镁的实验步骤如下: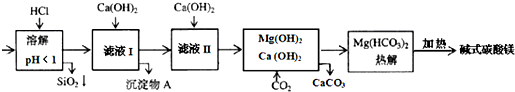
室温下,相关金属氢氧化物沉淀的KSP见下表
注:①lg2=0.3,②溶液中某离子的浓度小于1.0×10-5 mol•L-1,可认为该离子沉淀完全.
下列说法正确的是( )

室温下,相关金属氢氧化物沉淀的KSP见下表
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| (溶度积)KSP | 4.0×10-38 | 1.25×10-33 | 1.8×10-11 |
下列说法正确的是( )
| A. | 在滤液I中,加过量的Ca(OH)2使Fe3+和Al3+沉淀完全 | |
| B. | 滤液I中,加Ca(OH)2后Al3+比Fe3+先沉淀完全 | |
| C. | 室温下,用Ca(OH)2把滤液I的pH调节到4.7时,Al3+刚好沉淀完全 | |
| D. | 若碱式碳酸镁【aMgCO3•b Mg(OH)2】高温加热分解得到6.6g CO2和8.0g MgO,由此可知其化学式为MgCO3•3Mg(OH)2 |
12.六种短周期元素A、B、C、D、E、F的原子序数依次增大,其中A与E同主族,B与F同主族,E与F同周期.已知A与其他元素不在同一周期,D的核电荷数是B的最外层电子数的2倍,单质F是一种重要的半导体材料.则下列推断中正确的是( )
| A. | A、B两种元素可组成化学式为BA2的化合物 | |
| B. | F与D形成的化合物性质很不活泼,不与任何酸反应 | |
| C. | 原子半径由大到小的顺序是E>F | |
| D. | 气态氢化物的稳定性由强到弱的顺序是C>D |
2.下列叙述中正确的是( )
| A. | 可用丁达尔效应区别溶液和胶体 | B. | 稀硫酸不具有氧化性 | ||
| C. | 光导纤维的主要成分是硅 | D. | 石油的分馏属于化学变化 |
9.下列离子方程式中,正确的是( )
| A. | Al与NaOH溶液的反应:Al3++3OH-=Al (OH) 3↓ | |
| B. | CaCl2溶液与Na2CO3溶液反应:Ca2++CO32-=CaCO3↓ | |
| C. | MgSO4溶液与Ba(OH)2溶液反应:SO42-+Ba2+=BaSO4↓ | |
| D. | CaCO3与稀盐酸反应:CO32-+2 H+=H2CO3 |

