题目内容
(15分)氮的化合物在无机化工领域有着重要的地位。请回答下列问题:
(1)基态氮原子的价电子排布图为______。氮的最高价氧化物为无色晶体,它由两种离子构成:已知其阴离子构型为平面正三角形,则其阳离子的构型为 形,阳离子中氮的杂化轨道类型为 。
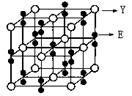
(2)某氮铝化合物X具有耐高温、抗冲击、导热性好等优良性质,广泛用于陶瓷工业等领域。工业上用氮气与氧化铝和碳在一定条件下反应生成X和CO,X的晶体结构如图所示,工业制备X的化学方程式为____。

(3)X晶体中包含的化学键类型为______。(填字母标号)
(4)已知氮化硼与X晶体类型相同,且氮化硼的熔点比X高,可能的原因是______
(5)若X的密度为pg/cm3,则晶体中最近的两个N原子的距离为______cm(阿伏加德罗常数用NA表示,不必化简)。
(1)基态氮原子的价电子排布图为______。氮的最高价氧化物为无色晶体,它由两种离子构成:已知其阴离子构型为平面正三角形,则其阳离子的构型为 形,阳离子中氮的杂化轨道类型为 。
(2)某氮铝化合物X具有耐高温、抗冲击、导热性好等优良性质,广泛用于陶瓷工业等领域。工业上用氮气与氧化铝和碳在一定条件下反应生成X和CO,X的晶体结构如图所示,工业制备X的化学方程式为____。

(3)X晶体中包含的化学键类型为______。(填字母标号)
| A.离子键 | B.共价键 | C.配位键 | D.金属键 |
(5)若X的密度为pg/cm3,则晶体中最近的两个N原子的距离为______cm(阿伏加德罗常数用NA表示,不必化简)。
(1) 直线 sp (2) Al2O3+N2+3C
直线 sp (2) Al2O3+N2+3C 2AlN+3CO (3)B、C
2AlN+3CO (3)B、C
(4)氮化硼与氮化铝均为原子晶体,且硼原子半径小于铝原子半径,B—N键键能大于Al—N键键能 (5)
 直线 sp (2) Al2O3+N2+3C
直线 sp (2) Al2O3+N2+3C 2AlN+3CO (3)B、C
2AlN+3CO (3)B、C(4)氮化硼与氮化铝均为原子晶体,且硼原子半径小于铝原子半径,B—N键键能大于Al—N键键能 (5)

试题分析:(1)7号元素N的核外电子排布式是1s22s22p3,所以基态氮原子的价电子排布图为
 ;氮的最高价氧化物N2O5为无色晶体,它由两种离子构成:NO2+(硝酰阳离子)和NO3-(硝酸根离子),其中阳离子呈直线型,阳离子中氮的杂化轨道类型为sp杂化,阴离子构型为平面正三角形; (2) 工业制备X的化学方程式为Al2O3+N2+3C
;氮的最高价氧化物N2O5为无色晶体,它由两种离子构成:NO2+(硝酰阳离子)和NO3-(硝酸根离子),其中阳离子呈直线型,阳离子中氮的杂化轨道类型为sp杂化,阴离子构型为平面正三角形; (2) 工业制备X的化学方程式为Al2O3+N2+3C 2AlN+3CO;(3)在AlN晶体中包含的化学键类型为共价键、配位键。因此选项为B、C。(4)已知氮化硼与AlN晶体类型相同,且氮化硼的熔点比AlN高,可能的原因是氮化硼与氮化铝均为原子晶体,且硼原子半径小于铝原子半径,使得B—N键的键能大于Al—N键的键能。(5)在每个晶胞中含有的Al原子的个数为:8×1/8+6×1/2=4;N:1×4=4.因此含有4个AlN。设晶胞的变成为L,则
2AlN+3CO;(3)在AlN晶体中包含的化学键类型为共价键、配位键。因此选项为B、C。(4)已知氮化硼与AlN晶体类型相同,且氮化硼的熔点比AlN高,可能的原因是氮化硼与氮化铝均为原子晶体,且硼原子半径小于铝原子半径,使得B—N键的键能大于Al—N键的键能。(5)在每个晶胞中含有的Al原子的个数为:8×1/8+6×1/2=4;N:1×4=4.因此含有4个AlN。设晶胞的变成为L,则 ;
; 则晶体中最近的两个N原子的距离为
则晶体中最近的两个N原子的距离为 cm。在晶胞中每个Al原子结合4个N原子,每个N原子结合4个Al原子,2个Al原子之间的距离与2个N原子的距离相等,都等于面对角线的一半,所以2个N原子之间的距离等于
cm。在晶胞中每个Al原子结合4个N原子,每个N原子结合4个Al原子,2个Al原子之间的距离与2个N原子的距离相等,都等于面对角线的一半,所以2个N原子之间的距离等于 。
。
练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
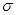 键 G.
键 G.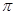 键
键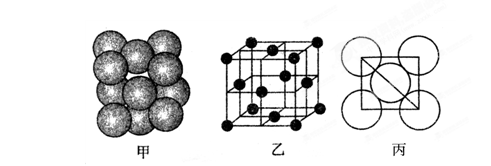
 = g/cm3。(用含M、NA、b的计算式表示,不用化简)。
= g/cm3。(用含M、NA、b的计算式表示,不用化简)。