题目内容
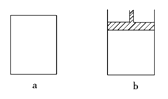
【题目】有两个极易导热的密闭容器a和b(如图所示),a容器体积恒定,b容器体积可变,压强不变。在同温同压和等体积条件下,向a和b两容器中通入等物质的量的NO2,发生反应:2NO2![]() N2O4(正反应放热),则以下说法正确的是
N2O4(正反应放热),则以下说法正确的是
A. 反应起始时反应速率的关系:va<vb
B. 反应过程中反应速率的关系:va<vb
C. 两容器内反应达到平衡所需时间一定相同
D. 反应达到平衡,两容器中的NO2的转化率相同
【答案】B
【解析】A.反应起始时两容器的反应速率va和vb的关系:va<vb错,起始瞬间,两容器体积相等,加入NO2相等,即浓度相等,即起始瞬间的速率相等,故A错误;B.反应过程中两容器内的反应速率va和vb的关系:va<vb正确,b的活塞会逐渐向下运动,即相当于加压,速率较a大,或者理解为b恒压,而a恒容,所以a中的压强会逐渐减小,速率相对较小,故B正确;C、两容器内反应达到平衡所需用的时间一定不等,因为速率不一样,平衡也不一样,故C错;D.反应达到平衡,两容器的NO2的转化率不相同,b容器较a相当于加压,所以平衡会正向移动,所以NO2的转化率比a大,故D错误;故选B。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
