题目内容
有关反应:4NH3(g)+5O2 (g)=4NO(g)+6H2O(g)△H=-905kJ/mol 的描述不正确的是( )
| A、生成物的总能量小于反应物的总能量 |
| B、该反应为吸热反应 |
| C、活化分子间的碰撞不一定是有效碰撞 |
| D、该反应中每4 mol NH3(g)被氧化,放出905 kJ热量 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:A、依据反应是放热反应,结合能量守恒分析判断;
B、反应焓变为负值,说明反应是放热反应;
C、反应物达到一定能量变为活化分子,发生的碰撞不一定是有效碰撞;
D、依据热化学方程式的定量关系计算得到放出的热量分析判断.
B、反应焓变为负值,说明反应是放热反应;
C、反应物达到一定能量变为活化分子,发生的碰撞不一定是有效碰撞;
D、依据热化学方程式的定量关系计算得到放出的热量分析判断.
解答:
解:A、4NH3 (g)+5O2 (g)═4NO(g)+6H2O(g)△H=-905kJ/mol,反应是放热反应,反应物能量高于生成物能量,故A正确;
B、4NH3(g)+5O2 (g)=4NO(g)+6H2O(g)△H=-905kJ/mol,焓变为负值是放热反应,故B错误;
C、活化分子间的碰撞发生化学反应的是有效碰撞,不反应的不是有效碰撞,活化分子间的碰撞不一定是有效碰撞,故C正确;
D、4NH3 (g)+5O2 (g)═4NO(g)+6H2O(g)△H=-905kJ/mol,反应中4mol氨气均被氧化,则4mol氨气被氧化放出905 kJ热量,故D正确;
故选B.
B、4NH3(g)+5O2 (g)=4NO(g)+6H2O(g)△H=-905kJ/mol,焓变为负值是放热反应,故B错误;
C、活化分子间的碰撞发生化学反应的是有效碰撞,不反应的不是有效碰撞,活化分子间的碰撞不一定是有效碰撞,故C正确;
D、4NH3 (g)+5O2 (g)═4NO(g)+6H2O(g)△H=-905kJ/mol,反应中4mol氨气均被氧化,则4mol氨气被氧化放出905 kJ热量,故D正确;
故选B.
点评:本题考查了热化学方程式的意义和表示方法,反应焓变的分析判断,题目较简单.

练习册系列答案
相关题目
下列表示对应化学反应的离子方程式正确的是( )
| A、过氧化钙固体与水反应:2O22-+2H2O═4OH-+O2↑ |
| B、用过氧化氢从酸化的海带灰浸出液中提取碘:2I-+H2O2+2H+═I2+2H2O |
| C、碳酸氢钙溶液中加入足量烧碱溶液:HCO3-+OH-═CO32-+H2O |
| D、AlCl3溶液中滴加浓氨水至过量:Al3++4NH3?H2O═AlO2-+4NH4++2H2O |
 目前,世界上已合成了几百种有机超导体,TCNQ是其中之一.TCNQ的分子结构如图所示.下列关于TCNQ说法错误的为( )
目前,世界上已合成了几百种有机超导体,TCNQ是其中之一.TCNQ的分子结构如图所示.下列关于TCNQ说法错误的为( )| A、分子中所有的氮原子在同一平面内 |
| B、属于芳香族化合物 |
| C、能发生加聚反应 |
| D、该物质难溶于水 |
工业上用含Fe2O3杂质的铝土矿为原料冶炼铝的工艺流程如下:下列叙述正确的是( )
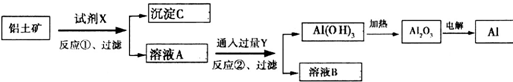

| A、反应①中试剂X是氢氧化钠溶液 |
| B、试剂Y是HCl,它与[Al(OH)4]-反应生成氢氧化铝 |
| C、图中所示转化反应中包含2个氧化还原反应 |
| D、将X与Y试剂进行对换,最终可以达到相同结果 |
下列说法正确的是( )
| A、向NaOH溶液中慢慢滴加FeCl3饱和溶液,可制得Fe(OH)3胶体 |
| B、胶体与其他分散系的本质区别是胶体能发生丁达尔效应 |
| C、Fe(OH)3胶体中的分散质为氢氧化铁分子 |
| D、向沸水中滴加FeCl3饱和溶液,加热至溶液变为红褐色,停止加热,制得氢氧化铁胶体 |
下列表述正确的是( )
A、羟基的电子式 |
| B、醛基的结构简式-COH |
C、1-丁烯的键线式 |
D、聚丙烯的结构简式 |
某溶液中存在大量的H+、Cl-、Fe3+,该溶液中还可能大量存在的离子是( )
| A、OHˉ |
| B、Ag+ |
| C、CO32- |
| D、SO42- |
某种蛋白酶由100个氨基酸脱水缩合而成,下列叙述正确的是( )
| A、该酶分子结构中至少含有99个氨基和99个羧基 |
| B、控制该酶合成的基因片段至少有300对碱基 |
| C、该酶从细胞中分泌出来需要载体的协助 |
| D、用含该酶的洗衣粉去除奶渍,效果比其他类型的加酶洗衣粉好 |