��Ŀ����
�����Ṥҵ�У�SO2ת��ΪSO3��һ���ؼ����裮
��1��SO2�����������л�ԭ�ԣ�����Ư���ԣ���SO2����ͨ������KMnO4��Һ�У���Һ��ɫ��SO2����______�ԣ������������ͻ�ԭ�����ʵ���֮��Ϊ______����֪KMnO4���������µĻ�ԭ����ΪMn2+����
��2��ij�¶��£�SO2��g��+
O2��g��?SO3��g������H=-98 kJ?mol-1����ʼʱ��100 L���ܱ������м���4.0 mol SO2��g����10.0 mol O2��g��������Ӧ�ﵽƽ��ʱ�ų�����196kJ�����¶���ƽ�ⳣ��K=______��
��3�����й���2SO2��g��+O2��g��?2SO3��g������H=-196kJ?mol-1��Ӧ����ͼ1ͼ���У��������______��
��4��һ�������£���һ���������ܱ������г���2 mol SO2��1 mol O2���������з�Ӧ��2SO2��g��+O2��g��?2SO3��g�����ﵽƽ���ı�����������SO2��O2��SO3����ƽ��Ũ�ȶ���ԭ���������______������ĸ����
A�������¶Ⱥ�����������䣬����2 mol SO3
B�������¶Ⱥ�����������䣬����2 mol N2
C�������¶Ⱥ�����������䣬����0.5 mol SO2��0.25 mol O2
D����������������䣬����������¶�
E���ƶ�����ѹ������
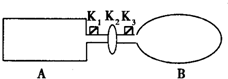
��5��ij����������ͼ2װ���������ᣬд��a�缫�ĵ缫��Ӧʽ______������SO42-�ľ������Ϊ______��
��1��SO2�����������л�ԭ�ԣ�����Ư���ԣ���SO2����ͨ������KMnO4��Һ�У���Һ��ɫ��SO2����______�ԣ������������ͻ�ԭ�����ʵ���֮��Ϊ______����֪KMnO4���������µĻ�ԭ����ΪMn2+����
��2��ij�¶��£�SO2��g��+
| 1 |
| 2 |
��3�����й���2SO2��g��+O2��g��?2SO3��g������H=-196kJ?mol-1��Ӧ����ͼ1ͼ���У��������______��

��4��һ�������£���һ���������ܱ������г���2 mol SO2��1 mol O2���������з�Ӧ��2SO2��g��+O2��g��?2SO3��g�����ﵽƽ���ı�����������SO2��O2��SO3����ƽ��Ũ�ȶ���ԭ���������______������ĸ����
A�������¶Ⱥ�����������䣬����2 mol SO3
B�������¶Ⱥ�����������䣬����2 mol N2
C�������¶Ⱥ�����������䣬����0.5 mol SO2��0.25 mol O2
D����������������䣬����������¶�
E���ƶ�����ѹ������
��5��ij����������ͼ2װ���������ᣬд��a�缫�ĵ缫��Ӧʽ______������SO42-�ľ������Ϊ______��

��1��SO2����ͨ������KMnO4�У�����KMnO4��ɫ�������������Ԫ������۾��������ԣ�����������л�ԭ�ԣ�MnԪ�ػ��ϼ���+7�۽��͵�+2�ۣ����ϼ۱仯5�ۣ�SԪ�ػ��ϼ���+4�����ߵ�+6�ۣ����ϼ۱仯2�ۣ�������ԭ��Ӧ���������ͻ�ԭ����ʧ������Ŀ��ȣ����������ͻ�ԭ�����ʵ���֮��Ϊ2��5��
�ʴ𰸣���ԭ��2��5��
��2��SO2��g��+
O2��g��?SO3��g������H=-98kJ?mol-1����100L���ܱ������м���4.0mol SO2��g����10.0molO2��g��������Ӧ�ﵽƽ��ʱ���ų�����196kJ��������SO2 2mol��
SO2��g��+
O2��g��?SO3��g������H=-98kJ?mol-1��
��ʼ 4.0mol 10.0mol 0
ת�� 2.0mol 1.0mol 2mol
ƽ�� 2.0mol 9.0mol 2mol
��ƽ��ʱ��c��SO2��=0.02mol/L��c��O2��=0.09mol/L��c��SO3��=0.02mol/L��
����k=
=3.33��
�ʴ�Ϊ��3.33��
��3��A�������¶ȣ��淴Ӧ����������࣬ƽ�����淴Ӧ�����ƶ���ͼ����ʵ�ʷ��ϣ���A��ȷ��
B�������¶ȣ�ƽ�����淴Ӧ�����ƶ�����������ĺ������ͣ�ͼ����ʵ�ʷ��ϣ���B��ȷ��
C�������¶ȣ��ӿ췴Ӧ���ʵ���ƽ����ʱ�����̣��淴Ӧ����������࣬ƽ�����淴Ӧ�����ƶ�����������ĺ������ͣ�ͼ����ʵ�ʲ�������C����
D������ѹǿ���ӿ췴Ӧ���ʵ���ƽ����ʱ�����̣�����Ӧ����������࣬ƽ��������Ӧ�����ƶ�����������ĺ�������ͼ����ʵ�ʷ��ϣ���D��ȷ��
�ʴ�Ϊ��C��
��4��A�������¶Ⱥ�����������䣬����2mol SO3��ƽ�����淴Ӧ�����ƶ�����SO2��O2��SO3����ƽ��Ũ�ȶ���ԭ������A��ȷ��
B�������¶Ⱥ�����������䣬����2mol N2����ƽ���ƶ�û��Ӱ�죬�����ʵ�Ũ�Ȳ��䣬��B����
C�������¶Ⱥ�����������䣬����0.5mol SO2��0.25mol O2��ƽ��������Ӧ�����ƶ�����SO2��O2��SO3����ƽ��Ũ�ȶ���ԭ������C��ȷ��
D�������¶ȣ�ƽ�����淴Ӧ�����ƶ���SO3��Ũ�ȼ�С����D����
E���ƶ�����ѹ�����壬�����С�������ʵ�Ũ�ȶ�����E��ȷ��
�ʴ�Ϊ��ACE��
��5������ͼװ�÷�������������ʧ���ӷ���������Ӧ��������������Ϊ������������ˮ�������ᣬ�缫��ӦΪ��SO2+2H2O-2e-=SO42-+4H+��������������ӵķ���Ϊ��ȡ������Һ���Թ��м������ᣬ�����������ټ���BaCl2��Һ����������ɫ����˵����Һ�к�SO42-��
�ʴ�Ϊ��SO2+2H2O-2e-=SO42-+4H+��ȡ������Һ���Թ��м������ᣬ�����������ټ���BaCl2��Һ��
�ʴ𰸣���ԭ��2��5��
��2��SO2��g��+
| 1 |
| 2 |
SO2��g��+
| 1 |
| 2 |
��ʼ 4.0mol 10.0mol 0
ת�� 2.0mol 1.0mol 2mol
ƽ�� 2.0mol 9.0mol 2mol
��ƽ��ʱ��c��SO2��=0.02mol/L��c��O2��=0.09mol/L��c��SO3��=0.02mol/L��
����k=
| 0.02 | ||
0.02��
|
�ʴ�Ϊ��3.33��
��3��A�������¶ȣ��淴Ӧ����������࣬ƽ�����淴Ӧ�����ƶ���ͼ����ʵ�ʷ��ϣ���A��ȷ��
B�������¶ȣ�ƽ�����淴Ӧ�����ƶ�����������ĺ������ͣ�ͼ����ʵ�ʷ��ϣ���B��ȷ��
C�������¶ȣ��ӿ췴Ӧ���ʵ���ƽ����ʱ�����̣��淴Ӧ����������࣬ƽ�����淴Ӧ�����ƶ�����������ĺ������ͣ�ͼ����ʵ�ʲ�������C����
D������ѹǿ���ӿ췴Ӧ���ʵ���ƽ����ʱ�����̣�����Ӧ����������࣬ƽ��������Ӧ�����ƶ�����������ĺ�������ͼ����ʵ�ʷ��ϣ���D��ȷ��
�ʴ�Ϊ��C��
��4��A�������¶Ⱥ�����������䣬����2mol SO3��ƽ�����淴Ӧ�����ƶ�����SO2��O2��SO3����ƽ��Ũ�ȶ���ԭ������A��ȷ��
B�������¶Ⱥ�����������䣬����2mol N2����ƽ���ƶ�û��Ӱ�죬�����ʵ�Ũ�Ȳ��䣬��B����
C�������¶Ⱥ�����������䣬����0.5mol SO2��0.25mol O2��ƽ��������Ӧ�����ƶ�����SO2��O2��SO3����ƽ��Ũ�ȶ���ԭ������C��ȷ��
D�������¶ȣ�ƽ�����淴Ӧ�����ƶ���SO3��Ũ�ȼ�С����D����
E���ƶ�����ѹ�����壬�����С�������ʵ�Ũ�ȶ�����E��ȷ��
�ʴ�Ϊ��ACE��
��5������ͼװ�÷�������������ʧ���ӷ���������Ӧ��������������Ϊ������������ˮ�������ᣬ�缫��ӦΪ��SO2+2H2O-2e-=SO42-+4H+��������������ӵķ���Ϊ��ȡ������Һ���Թ��м������ᣬ�����������ټ���BaCl2��Һ����������ɫ����˵����Һ�к�SO42-��
�ʴ�Ϊ��SO2+2H2O-2e-=SO42-+4H+��ȡ������Һ���Թ��м������ᣬ�����������ټ���BaCl2��Һ��

��ϰ��ϵ�д�
 ����ѧҵ���Ե�����ϵ�д�
����ѧҵ���Ե�����ϵ�д�
�����Ŀ