题目内容
Ⅰ、CO和H2的混合气体俗称合成气,是一种重要的工业原料气,焦炭、天然气(主要成分为CH4)、重油、煤在高温下均可与水蒸气反应制得合成气.
(1)已知某反应的平衡常数表达式为:K=
,它所对应的化学方程式为:______.
(2)向体积为2L的密闭容器中充入CH4和H2O(g)组成的混合气(共1mol),在一定条件下发生反应,并达到平衡状态,测得温度、压强、投料比X〔
)对该反应的影响如图所示.
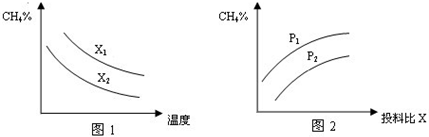
①图1中的两条曲线所示投料比的关系X2______X1(填“=”“>”或“<”下同)
②图2中两条曲线所示的压强比的关系:P2______P1
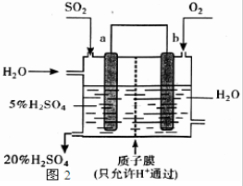
(3)以CH4、O2为原料可设计成燃料电池:
①设装置中盛有150.0mL1.0mol/LKOH溶液,放电时参与反应的氧气在标准状况下的体积为4.48L,放电过程中转移电子的物质的量为______.
②以H2SO4溶液代替KOH溶液为电解质溶液,则燃料电池的负极反应式为:______.
Ⅱ、(1)有一种用CO2生产甲醇燃料的方法:
已知:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-akJ?mol-1;
CH3OH(g)═CH3OH(l)△H=-bkJ?mol-1;
2H2(g)+O2(g)═2H2O(g)△H=-ckJ?mol-1;
H2O(g)═H2O(l)△H=-dkJ?mol-1,
则表示CH3OH(l)燃烧热的热化学方程式为:______.
(2)已知某温度下Mg(OH)2的Ksp=6.4xl0-12,当溶液中c(Mg2+)≤1.0×10-5mol?L-1可视为沉淀完全,则应保持溶液中c(OH-)≥______mol?L-1.
(1)已知某反应的平衡常数表达式为:K=
| c(H2)?c(CO) |
| c(H2O) |
(2)向体积为2L的密闭容器中充入CH4和H2O(g)组成的混合气(共1mol),在一定条件下发生反应,并达到平衡状态,测得温度、压强、投料比X〔
| n(CH4) |
| n(H2O) |

①图1中的两条曲线所示投料比的关系X2______X1(填“=”“>”或“<”下同)
②图2中两条曲线所示的压强比的关系:P2______P1
(3)以CH4、O2为原料可设计成燃料电池:
①设装置中盛有150.0mL1.0mol/LKOH溶液,放电时参与反应的氧气在标准状况下的体积为4.48L,放电过程中转移电子的物质的量为______.
②以H2SO4溶液代替KOH溶液为电解质溶液,则燃料电池的负极反应式为:______.
Ⅱ、(1)有一种用CO2生产甲醇燃料的方法:
已知:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-akJ?mol-1;
CH3OH(g)═CH3OH(l)△H=-bkJ?mol-1;
2H2(g)+O2(g)═2H2O(g)△H=-ckJ?mol-1;
H2O(g)═H2O(l)△H=-dkJ?mol-1,
则表示CH3OH(l)燃烧热的热化学方程式为:______.
(2)已知某温度下Mg(OH)2的Ksp=6.4xl0-12,当溶液中c(Mg2+)≤1.0×10-5mol?L-1可视为沉淀完全,则应保持溶液中c(OH-)≥______mol?L-1.
Ⅰ、(1)平衡表达式为:K=
,生成物为CO、H2,反应物含有H2O,三者化学计量数分别为1、1、1,根据元素守恒,故另一反应物为固体C,反应中它所对应反应的化学方程式为C(s)+H2O(g)?CO(g)+H2(g),
故答案为:C(s)+H2O(g)?CO(g)+H2(g);
(2)CH4(g)+H2O(g)=CO(g)+3H2(g);
①碳水比
值越大,平衡时甲烷的转化率越低,含量越高,故x2<x1,故答案为:<;
②该反应正反应是气体体积增大的反应,增大压强平衡向逆反应方向移动,平衡时甲烷的含量增大,故p2<p1,故答案为:<;
(3)①参与反应的氧气在标准状况下体积为4.48L,物质的量为
=0.2mol,氢转移电子的物质的量为0.2mol×4=0.8mol,故答案为:0.8mol;
②以H2SO4溶液代替KOH溶液为电解质溶液,失电子的做负极发生氧化反应,CH4+2H2O-8e-=CO2+8H+,故答案为:CH4+2H2O-8e-=CO2+8H+;
Ⅱ、(1)已知①CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-a kJ?mol-1;
②CH3OH(g)═CH3OH(l)△H=-b kJ?mol-1;
③2H2(g)+O2(g)═2H2O(g)△H=-c kJ?mol-1;
④H2O(g)═H2O(l)△H=-d kJ?mol-1,
由盖斯定律,(-①×2-②×2+③×3+④×4)÷2得CH3OH(l)+
O2(g)=CO2(g)+2H2O(l),故△H=(a+b-
c-2d) kJ∕mol,
故答案为:CH3OH(l)+
O2(g)=CO2(g)+2H2O(l),故△H=(a+b-
c-2d) kJ∕mol;
(2)Mg(OH)2的Ksp=6.4×10-12,当溶液中c(Mg2+)≤1.0×10-5mol?L-1可视为沉淀完全,则Ksp=c(Mg2+)×c2(OH-)=6.4×10-12 ,c(OH-)≥8×10-4mol/L,故答案为:8×10-4.
| c(H2)?c(CO) |
| c(H2O) |
故答案为:C(s)+H2O(g)?CO(g)+H2(g);
(2)CH4(g)+H2O(g)=CO(g)+3H2(g);
①碳水比
| n(CH4) |
| n(H2O) |
②该反应正反应是气体体积增大的反应,增大压强平衡向逆反应方向移动,平衡时甲烷的含量增大,故p2<p1,故答案为:<;
(3)①参与反应的氧气在标准状况下体积为4.48L,物质的量为
| 4.48L |
| 22.4L/mol |
②以H2SO4溶液代替KOH溶液为电解质溶液,失电子的做负极发生氧化反应,CH4+2H2O-8e-=CO2+8H+,故答案为:CH4+2H2O-8e-=CO2+8H+;
Ⅱ、(1)已知①CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-a kJ?mol-1;
②CH3OH(g)═CH3OH(l)△H=-b kJ?mol-1;
③2H2(g)+O2(g)═2H2O(g)△H=-c kJ?mol-1;
④H2O(g)═H2O(l)△H=-d kJ?mol-1,
由盖斯定律,(-①×2-②×2+③×3+④×4)÷2得CH3OH(l)+
| 3 |
| 2 |
| 3 |
| 2 |
故答案为:CH3OH(l)+
| 3 |
| 2 |
| 3 |
| 2 |
(2)Mg(OH)2的Ksp=6.4×10-12,当溶液中c(Mg2+)≤1.0×10-5mol?L-1可视为沉淀完全,则Ksp=c(Mg2+)×c2(OH-)=6.4×10-12 ,c(OH-)≥8×10-4mol/L,故答案为:8×10-4.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目