题目内容
 据某媒体报道:国家质检总局2011年12月24日公布了对200种液体乳产品质量的抽查结果.发现蒙牛、长富纯牛奶两种产品黄曲霉毒素M1项目不符合标准的规定.已知黄曲霉毒素(AFTB)分子结构式为如图所示.人体的特殊基因在黄曲霉素的作用下会发生突变,有转变为肝癌的可能.一般条件下跟1mol AFTB起反应的H2或NaOH的最大量分别是( )
据某媒体报道:国家质检总局2011年12月24日公布了对200种液体乳产品质量的抽查结果.发现蒙牛、长富纯牛奶两种产品黄曲霉毒素M1项目不符合标准的规定.已知黄曲霉毒素(AFTB)分子结构式为如图所示.人体的特殊基因在黄曲霉素的作用下会发生突变,有转变为肝癌的可能.一般条件下跟1mol AFTB起反应的H2或NaOH的最大量分别是( )| A、6mol;1mol |
| B、5mol;1mol |
| C、6mol;2mol |
| D、5mol;2mol |
考点:有机物的结构和性质
专题:
分析:分子中含有碳碳双键、羰基和苯环,都可与氢气是加成反应,含有酯基,可在碱性条件下水解,水解生成羧基和酚羟基,以此解答该题.
解答:
解:黄曲霉毒素(AFTB)含有1个-COO-,水解可生成-COOH和酚羟基,二者都可与NaOH反应,则1mol黄曲霉毒素消耗2molNaOH,分子中含有2个C=C、1个 和1个苯环,都可与氢气发生加成反应,所以1mol黄曲霉毒素可与6molH2发生加成反应,
和1个苯环,都可与氢气发生加成反应,所以1mol黄曲霉毒素可与6molH2发生加成反应,
故选C.
 和1个苯环,都可与氢气发生加成反应,所以1mol黄曲霉毒素可与6molH2发生加成反应,
和1个苯环,都可与氢气发生加成反应,所以1mol黄曲霉毒素可与6molH2发生加成反应,故选C.
点评:本题考查有机物的结构和性质,为高频考点,注意分析有机物中官能团的种类和性质,特别要注意-COO-中虽含C=O键,但不能与氢气发生加成反应,题目难度中等.

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案
相关题目
PHB塑料是一种可在微生物作用下降解的环保型塑料,其结构简式为: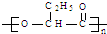 .下面有关PHB说法中,不正确的是( )
.下面有关PHB说法中,不正确的是( )
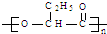 .下面有关PHB说法中,不正确的是( )
.下面有关PHB说法中,不正确的是( )| A、PHB是一种聚酯 |
| B、合成PHB的单体是CH3CH2CH(OH)COOH |
| C、PHB的降解产物可能有CO2和H2O |
| D、PHB通过加聚反应制得 |
下列有机物在H-NMR(氢的核磁共振谱图)上只给出一组峰的是( )
| A、HCHO |
| B、CH3OCH2CH3 |
| C、HCOOH |
| D、CH3COOCH3 |
下列图示与对应的叙述不相符合的是( )


| A、图1(图中→代表一步反应完成)中a、b、c分别代表FeCl2、Fe(OH)2、Fe(OH)3之间的相互转化关系 |
| B、图2表示在含等物质的量的NaHCO3、Na2CO3的混合溶液中滴加0.1 mol/L盐酸至过量时,产生气体物质的量与盐酸体积的关系 |
| C、图3表示向NaOH、Ba(OH)2、NaAlO2的混合溶液中不断通入CO2时沉淀的物质的量与通入CO2的体积的关系 |
| D、图4的装置既可用来证明KMnO4、Cl2、FeCl3的氧化性强弱顺序为KMnO4>Cl2>FeCl3;也可用来证明盐酸、碳酸、硅酸的酸性强弱顺序为HCl>H2CO3>H2SiO3[已知2KMnO4+16HCl=5KCl+2MnCl2+5Cl2↑+8H2O] |
下列叙述正确的是( )
| A、0.1mol?L-1氨水中,c(OH-)=c(NH4+) |
| B、10 mL 0.02mol?L-1HCl溶液与10 mL 0.02mol?L-1Ba(OH)2溶液充分混合,若混合后溶液的体积为20 mL,则溶液的pH=10 |
| C、在0.1mol?L-1CH3COONa溶液中,c(OH-)=c(CH3COOH)+c(H+) |
| D、0.1mol?L-1某二元弱酸强碱盐NaHA溶液中,c(Na+)=2c(A2-)+c(HA-)+c(H2A) |
短周期元素X、Y、Z的原子序数依次增大,其原子的最外层电子数之和为13.X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍或者Y原子最外层电子数的3倍,下列说法不正确的是( )
| A、X的最高价氧化物对应的水化物可表示为H2XO4 |
| B、X与Y形成的化合物的化学式是X2Y3 |
| C、Z的氢化物的沸点比上一周期的同族元素的氢化物的沸点低,其主要原因是Z的氢化物分子中不含氢键 |
| D、Y的氧化物的晶体是离子晶体 |
某温度下,体积固定的密闭容器中进行如下可逆反应:X(g)+Y(g)?Z(g)+W(s)△H>0,下列叙述正确的是( )
| A、当容器中气体的密度不变时,反应达到平衡 |
| B、加入少量W,逆反应速率增大 |
| C、升高温度,Y的百分含量增加 |
| D、平衡后加入X,上述反应的△H增大 |