题目内容
6. 硫酸的年产量高低常用于衡量一个国家化工生产水平的高低.
硫酸的年产量高低常用于衡量一个国家化工生产水平的高低.(1)以黄铁矿为原料生产SO2时反应的化学方程式为:4FeS2 +11 O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2,该反应在沸腾炉中进行(填设备名称);
(2)某科研小组测得某硫酸工厂生产工厂中SO2的平衡转化率与外部条件的关系如下表所示,则生产过程中,最适合的生产条件是1个大气压、400℃;
| 压强 (Pa) 温度 (℃) | 1.013×105 | 5.065×105 | 10.13×105 | 15.195×105 |
| 400 | 99.61% | 99.72% | 99.84% | 99.88×105 |
| 500 | 96.75% | 97.67% | 98.52% | 98.94% |
| 600 | 85.20% | 88.97% | 92.76% | 94.68% |
(4)下列做法中,与提高硫酸工业的经济效益无关的是d;
a.适当地对黄铁矿进行粉碎
b.在接触室中使用适当过量的O2
c.利用生产中的余热发电或供暖
d.对废水进行无害化处理后再排放
(5)硫酸工业会产生许多对环境有害的物质,因此无论是工厂厂址的选择还是生产过程中有害成分的处理都要充分考虑环保的要求;
①某市计划建一个硫酸工厂,厂址有A、B、C三个地方可供选择,假设最终该厂建在B地,你认为选择B地建厂的理由是(至少回答两点)B地远离硫酸的消耗中心、B地远离人品稠密的地方;
②将尾气中SO2在一定条件下转化为CaSO4,然后利用焦炭将其转化为CaS(另有一种可燃性气体生成)具有重要的意义,写出CaSO4转化为CaS的化学方程式CaSO4+4C$\frac{\underline{\;高温\;}}{\;}$CaS+4CO;
(6)若用等质量的硫磺,FeS2生产硫酸,假设原料的总利用率均为90%,则二者得到的硫酸质量比为15:8.
分析 (1)工业制硫酸是在沸腾炉中燃烧黄铁矿,黄铁矿的主要成分是FeS2,在氧气中燃烧得到SO2和Fe2O3;
(2)接触室发生的反应为2SO2(g)+O2(g)?△2SO3(g)△H<0,升高温度平衡逆向移动,反应物的转化率降低,从图表中可以看出,恒温时增大压强平衡正向移动,但反应物的转化率变化幅度不大,但压强的增大消耗能源及对设备的要求也高,故不易高压,综合考虑可选择适宜温度和压强;
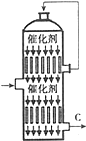
(3)接触室发生的反应为2SO2(g)+O2(g)?△2SO3(g)△H<0,反应放出的热量会使容器内温度升高,促进平衡逆向移动,不易提高反应的转化率,故通过热交换器对反应降温,转移能量给反应物加热;从C处排出的尾气主要含有SO2和SO3,其中SO3能和BaCl2溶液反应生成白色沉淀,SO2不能与反应,原因是弱酸不能制强酸;
(4)矿石粉碎后有利于硫元素尽可能多转化为SO2及提高反应速率,a正确;氧气过量可提高SO2的转化率,b正确;余热发电或供暖可“变废为宝”,c正确;废液处理会导致投入增加,d错误;
(5)①由于运送硫酸的成本远高于运送矿石的成本,故硫酸工厂应该接近消耗中心的地方;又因为硫酸属于重污染工业,故应建在远离风景名胜区,人口稠密的地方;②C与CaSO4是反应物,生成物是CO与CaS,由此可写出对应的化学方程式;
(6)化学变化过程中遵守原子守恒①,可以先计算出等质量的硫磺和FeS2的物质的量之比,即可计算出生成硫酸的物质的量比及硫酸的质量比.
解答 解:(1)工业制硫酸是利用黄铁矿在沸腾炉中燃烧生成二氧化硫,然后在接触室催化氧化二氧化硫得三氧化硫,最后吸收塔用98%的浓硫酸吸收SO3,其中黄铁矿燃烧反应方程式为4FeS2 +11 O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2,故答案为:4FeS2 +11 O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2;沸腾炉;
(2)从图中可看出恒压条件下升高温度,SO2的转化率降低,因此选择低温400℃,在恒温条件下增大压强,SO2的转化率增大幅度较小,考虑到产生高压会消耗能源及对设备的要求较高,因此选择较低压强为宜,故答案为:1个大气压、400℃;
(3)在接触室内通过热交换转移反应放出的热量,给容器降温,促进平衡正向移动提高SO2的转化率,另外通过热交换可以给反应物预热,有利于反应进行;从C处排出的尾气主要含有SO2和SO3,通过BaCl2溶液时,SO3能和BaCl2溶液反应生成BaSO4沉淀,SO2不能被吸收,发生反应的离子方程式为SO3+Ba2++H2O=BaSO4↓+2H+,故答案为:预热原料气,吸收反应放出的热量;SO3+Ba2++H2O=BaSO4↓+2H+;
(4)a.粉碎黄铁矿增大反应接触面积,有利于提高硫原子利用率,a正确;
b.在接触室中使用适当过量的O2,可提高SO2的转化率,对提高硫酸的产量有利,b正确;
c.通过热交换可将反应产生的热量转移出来用于余热发电或供暖,提高经济效益,c正确;
d.对废水进行无害化处理后再排放,避免环境污染,但增加了经济反投入,d错误;
故答案为:d;
(5)①工业制硫酸选择厂址时要考虑原料的运输成本,因尾气对环境有影响应尽量避免对居民的生活影响,减少对名胜古迹的损害,综合考虑B地完全符合条件,适宜建厂;②焦炭将CaSO4转化为CaS和另有一种可燃性气体生成,结合化学反应的本质,可知此气体是CO,发生反应的化学方程式为CaSO4+4C$\frac{\underline{\;高温\;}}{\;}$CaS+4CO↑;故答案为:①B地远离硫酸的消耗中心,B地远离人品稠密的地方,B地不发球风景名胜区;②CaSO4+4C$\frac{\underline{\;高温\;}}{\;}$CaS+4CO↑;
(6)已知n=$\frac{mg}{Mg/mol}$,可知等质量的硫磺和FeS2的物质的量之比与二者摩尔质量之比成反比,则硫磺和FeS2的物质的量之比为$\frac{120g/mol}{32g/mol}=\frac{15}{4}$,在制备硫酸的过程中遵守硫原子守恒,且生成硫酸的质量比等于物质的量之比为$\frac{15}{4×2}$=15:8;故答案为:15:8.
点评 硫酸工业制法,考查氧化还原理论,化学平衡的移动,原子守恒等知识点,对学生的基础要求比较强,属中等难度.

方法一、还原法:在酸性介质中用FeSO4、NaHSO3等将+6价Cr还原成+3价Cr.具体流程如下:

有关离子完全沉淀的pH如下表.
| Fe(OH)2 | Fe(OH)3 | Cr(OH)3 | |
| Ksp | 8.0×10-16 | 4.0×10-38 | 6.0×10-31 |
| 完全沉淀的pH | 9.0 | 3.2 | 5.6 |
(1)在②中调节pH的范围至B为最好.(填序号)
A.3~4 B.6~8 C.10~11 D.12~14
(2)若在①使FeSO4适当过量、空气适量,使Fe2+与Fe3+的比例恰当时,可产生具有磁性、组成类似于Fe3O4•xH2O的铁氧体悬浮物,变废为宝.则控制空气适量的目的是使溶液中Fe2+与Fe3+的比例恰当,使铁氧体分离出来较简便的方法是用磁铁吸引.
方法二、电解法:将含+6价Cr的废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解:阳极区生成的Fe2+和Cr2O72-发生反应,生成的Fe3+和Cr3十在阴极区与OH一结合生成Fe(OH)3和Cr(OH)3沉淀除去.
(3)写出此阴极反应的电极方程式2H2O+2e-═H2↑+2OH-.现用上法处理1×104 L含铬(+6价)78mg/L的废水,电解时阳极物质消耗的质量至少为2.52kg.
(1)已知:Fe2O3(s)+3C(s)═2Fe(s)+3CO(g)△H1=+489.0kJ•mol-1,
C(s)+CO2(g)═2CO(g)△H2=+172.5kJ•mol-1
则CO还原Fe2O3(s)的热化学方程式为Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H=-28.5kJ/mol.
(2)CO2和H2充入一定体积的密闭容器中,
在两种温度下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
测得CH3OH的物质的量随时间的变化见图1.
①曲线I、Ⅱ对应的平衡常数大小关系为KⅠ> KⅡ(填“>”或“=”或“<”).
②一定温度下,在容积相同且固定的两个密闭容器中,按如下方式加入反应物,一段时间后达到平衡.
| 容 器 | 甲 | 乙 |
| 反应物投入量 | 1molCO2、3molH2 | a molCO2、b molH2、 c molCH3OH(g)、c molH2O(g) |
(3)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2.紫外光照射时,在不同催化剂(I、II、III)作用下,CH4产量随光照时间的变化见图2.在0~15小时内,CH4的平均生成速率I、II和III从大到小的顺序为II>III>I(填序号).
(4)以TiO2/Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸.在不同温度下催化剂的催化效率与乙酸的生成速率的关系见图3.
①乙酸的生成速率主要取决于温度影响的范围是300℃~400℃.
②Cu2Al2O4可溶于稀硝酸,写出有关的离子方程式:3Cu2Al2O4+32H++2NO3-=6Cu2++6Al3++2NO↑+16H2O.

| A. | 3He和4He | B. | 乙烷和乙烯 | ||
| C. | 乙醇和二甲醚(CH3OCH3) | D. | O2和O3 |
| A. | 纳米碳管是一种新型的高分子化合物 | |
| B. | 纳米碳管的化学性质稳定 | |
| C. | 纳米碳管的结构和性质与金刚石相同 | |
| D. | 纳米碳管导电属于化学变化 |
| A. | NA个OH-含有电子10mol | |
| B. | 某元素R一个原子的质量是ag,则其的相对原子质量可表示为a NA | |
| C. | 4L0.5mol/L的NaOH溶液中含有阴离子的数目为2NA | |
| D. | 配制一定物质的量浓度的NaOH溶液时,定容时俯视操作所得溶液浓度偏低 |



