��Ŀ����
��ͼ�Ǽ״�ȼ�ϵ�صĹ���ʾ��ͼ���õ���ܷ�ӦʽΪ��2CH3OH+3O2=2CO2+4H2O�������йظõ�ص�˵������ȷ����( )
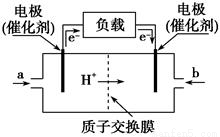
A�������ļ״�ͨ��ȼ�ϵ���ͷŵĵ��ܱ���ͨ��������������ĵ��ܶ�
B����ߵĵ缫Ϊ��صĸ�����a��ͨ����Ǽ״�
C����ظ����ķ�ӦʽΪ��2CH3OH+2H2O-12e��=2CO2��+12H��
D�����óص�ص����������ʳ��ˮ(ʯī�缫)������1mol�״�ʱ�����������44.8L����
 Ŀ�����ϵ�д�
Ŀ�����ϵ�д���Ҫ��ش��������⣺
(1)����FeCl3��Һʱ���轫�������ڽ�Ũ���������Ҫ����ϡ�ͣ������ӷ���ʽ������ԭ�� ��
(2)�����ӷ���ʽ��ʾ����ĭ�������ԭ�� ��
(3)ʵ�����г���NaOH��Һ������ϴ�����ᴿ����100mL 3mol��L-1��NaOH��Һ���ձ�״����4��48LCO2ʱ��������Һ������Ũ���ɴ�С��˳��Ϊ ��
(4)�����£�Ũ�Ⱦ�Ϊ0.1mol/L������������Һ��PHֵ���±���ʾ��
���� | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
�ٸ��ݱ������ݣ���Ũ�Ⱦ�Ϊ0.01mol�� L-1���������������Һ�ֱ�ϡ��100����pH�仯��С���� ��
A��HCN B��HClO C��H2CO3 D��CH3COOH
�ڸ����������ݣ��ж����з�Ӧ���Գ������� ��
A��CH3COOH+Na2CO3�TNaHCO3+CH3COONa
B��CH3COOH+NaCN�TCH3COONa+HCN
C��CO2+H2O+2NaClO�TNa2CO3+2HClO
D��NaHCO3+HCN�TNaCN+H2O+CO2
(5)��֪��Cu2����Mg2����Fe2��Ũ����ͬ����Һ�У��俪ʼ����ʱ��pH���£�
���� | Fe2+ | Cu2+ | Mg2+ |
pH | 7.6 | 5.2 | 10.4 |
�������Һ�еμ�NaOH��Һ�����ȳ������� (�����ӷ���)��
�ж�Ksp[Fe(OH)2] Ksp[Mg(OH)2](���������=������)��
��֪Ksp[Cu(OH)2]=2.5��10-20���������Һ�м�����ʯ�ҵ�����pH����pH= ʱ����Һ��Cu2+������ȫ��[��֪1g2=0.3]
�������ʵ���������ʵ���������( )
ѡ�� | A | B | C | D |
���� | �������� | ���� | ���� | �������� |
��ʵ | pH>7 | ����ˮ�������� | �ɲ�������ЧӦ������ | ����ʳƷ������ |


 2ClO2����K2SO4��2CO2����2H2O������˵����ȷ����( )
2ClO2����K2SO4��2CO2����2H2O������˵����ȷ����( ) l����ת��
l����ת��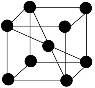 ,Z���ӵİ뾶Ϊd cm,��Z���ʵ��ܶ�Ϊ_______��
,Z���ӵİ뾶Ϊd cm,��Z���ʵ��ܶ�Ϊ_______��