��Ŀ����
��Ҫ��ش��������⣺
(1)����FeCl3��Һʱ���轫�������ڽ�Ũ���������Ҫ����ϡ�ͣ������ӷ���ʽ������ԭ�� ��
(2)�����ӷ���ʽ��ʾ����ĭ�������ԭ�� ��
(3)ʵ�����г���NaOH��Һ������ϴ�����ᴿ����100mL 3mol��L-1��NaOH��Һ���ձ�״����4��48LCO2ʱ��������Һ������Ũ���ɴ�С��˳��Ϊ ��
(4)�����£�Ũ�Ⱦ�Ϊ0.1mol/L������������Һ��PHֵ���±���ʾ��
���� | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
�ٸ��ݱ������ݣ���Ũ�Ⱦ�Ϊ0.01mol�� L-1���������������Һ�ֱ�ϡ��100����pH�仯��С���� ��
A��HCN B��HClO C��H2CO3 D��CH3COOH
�ڸ����������ݣ��ж����з�Ӧ���Գ������� ��
A��CH3COOH+Na2CO3�TNaHCO3+CH3COONa
B��CH3COOH+NaCN�TCH3COONa+HCN
C��CO2+H2O+2NaClO�TNa2CO3+2HClO
D��NaHCO3+HCN�TNaCN+H2O+CO2
(5)��֪��Cu2����Mg2����Fe2��Ũ����ͬ����Һ�У��俪ʼ����ʱ��pH���£�
���� | Fe2+ | Cu2+ | Mg2+ |
pH | 7.6 | 5.2 | 10.4 |
�������Һ�еμ�NaOH��Һ�����ȳ������� (�����ӷ���)��
�ж�Ksp[Fe(OH)2] Ksp[Mg(OH)2](���������=������)��
��֪Ksp[Cu(OH)2]=2.5��10-20���������Һ�м�����ʯ�ҵ�����pH����pH= ʱ����Һ��Cu2+������ȫ��[��֪1g2=0.3]
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����ͼ����ȡ�������������������������װ��ʾ��ͼ����������װ�ý����±�����ʵ�飬�ܴﵽʵ��Ŀ�ĵ���( )
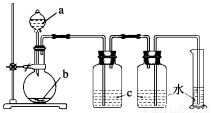
���� ʵ�� | a(Һ��) | b(����) | c(Һ��) |
A | ϡ���� | п�� | Ũ���� |
B | Ũ��ˮ | ��ʯ�� | Ũ���� |
C | Ũ���� | CuƬ | NaOH��Һ |
D | ϡ���� | CuƬ | H2O |


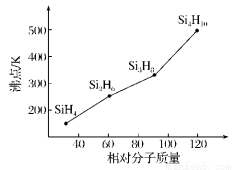
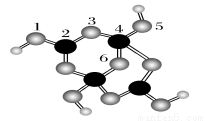

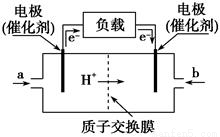
 2CrO42-(��ɫ)+2H+ ����K2Cr2O7��Һ��������ʵ�飬���ʵ�飬����˵������ȷ���ǣ� ��
2CrO42-(��ɫ)+2H+ ����K2Cr2O7��Һ��������ʵ�飬���ʵ�飬����˵������ȷ���ǣ� ��