��Ŀ����
2��A��B��C��D��E���ֶ�����Ԫ�أ�A��Bͬ���壬C��Dͬ���ڣ�B��Eͬ���ڣ�����A2������C2��Ϻ��ȼ�ܹ�������ը���Ҳ����ڳ��³�ѹ����һ����ɫ��ζ��Һ�壮B��C��E�����ӵĺ�������Ų���ͬ��E��������������B������������ˮ���ﷴӦ����һ��������ˮ���Σ�D���γ���Ȼ��Ӳ�����ĵ��ʣ�������������ṩ����Ϣ�ش��������⣮��1��д��A��B����Ԫ�ص�Ԫ�����ƣ�A�⡢B�ƣ�д��D�����������ĵ���ʽ
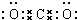 ��
����2��д����B��C��Ԫ���γɵ�ԭ�Ӹ�����Ϊ1��1�Ļ�����F�ĵ���ʽ
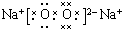 ������ڵĻ�ѧ�������Ӽ��ͷǼ��Լ�
������ڵĻ�ѧ�������Ӽ��ͷǼ��Լ���3��д��F��A2C��Ӧ�����ӷ���ʽ��2Na2O2+H2O=4Na++4OH-+O2����
��4���õ���ʽ��ʾB2C�γɵĹ��̣�
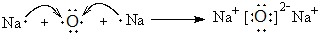 ��
��
���� ����A2������C2��Ϻ��ȼ�ܹ�������ը���Ҳ����ڳ��³�ѹ����һ����ɫ��ζ��Һ�壬��A��CΪH��OԪ�ص�һ�֣�B��C��E�����ӵĺ�������Ų���ͬ����CΪOԪ�أ���AΪHԪ�أ�D���γ���Ȼ��Ӳ�����ĵ��ʣ���DΪCԪ�أ�A��Bͬ���壬��C��E������ͬ�ĺ�������Ų�����BΪNaԪ�أ��ݴ˽��Ԫ��������֪ʶ���
��� �⣺����A2������C2��Ϻ��ȼ�ܹ�������ը���Ҳ����ڳ��³�ѹ����һ����ɫ��ζ��Һ�壬��A��CΪH��OԪ�ص�һ�֣�B��C��E�����ӵĺ�������Ų���ͬ����CΪOԪ�أ���AΪHԪ�أ�D���γ���Ȼ��Ӳ�����ĵ��ʣ���DΪCԪ�أ�A��Bͬ���壬��C��E������ͬ�ĺ�������Ų�����BΪNaԪ�أ�
��1�����ݷ�����֪��A��B�ֱ�Ϊ�⡢��Ԫ�أ�DΪCԪ�أ������������Ϊ������̼��������̼Ϊ���ۻ���������ʽΪ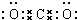 ��
��
�ʴ�Ϊ���⣻�ƣ�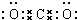 ��
��
��2��B��C�ֱ�ΪNa��OԪ�أ���B��C��Ԫ���γɵ�ԭ�Ӹ�����Ϊ1��1�Ļ�����FΪ�������ƣ���������Ϊ���ӻ������ĵ���ʽΪ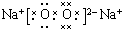 �����������к������Ӽ��ͷǼ��Լ���
�����������к������Ӽ��ͷǼ��Լ���
�ʴ�Ϊ��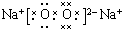 �����Ӽ��ͷǼ��Լ���
�����Ӽ��ͷǼ��Լ���
��3��FΪ�������ƣ�A2CΪˮ������������ˮ��Ӧ�����ӷ���ʽΪ��2Na2O2+H2O=4Na++4OH-+O2����
�ʴ�Ϊ��2Na2O2+H2O=4Na++4OH-+O2����
��4��B2CΪNa2O���õ���ʽ��ʾ�����Ƶ��γɹ���Ϊ��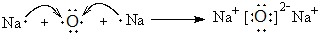 ��
��
�ʴ�Ϊ��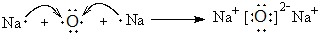 ��
��
���� ���⿼����λ�á��ṹ�����ʹ�ϵ���ۺ�Ӧ�ã���Ŀ�Ѷ��еȣ��ƶ�Ԫ��Ϊ���ؼ���ע�����ճ�����ѧ����ı�ʾ��������ȷԭ�ӽṹ��Ԫ�������ɡ�Ԫ�����ڱ��Ĺ�ϵ��

 �����Ļ�������ҵϵ�д�
�����Ļ�������ҵϵ�д� ����������������ϵ�д�
����������������ϵ�д�| A�� | 4molA+2molB | B�� | 1.5molC+0.5molD | ||
| C�� | 1molB+1molD | D�� | 1molA+0.5molB+1.5molC+0.5molD |
| A�� | ˮ���� | B�� | �Ȼ��� | C�� | ���� | D�� | �������� |
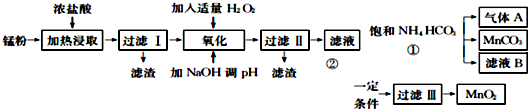
��֪�����������↑ʼ��������ȫ������pH�����
| �������� | Fe��OH�� | Fe��OH�� | Mn0H��2 | Zn��OH��2 |
| ��ʼ������pH | 7.5 | 2.2 | 8.8 | 6.4 |
| ������ȫ��pH | 9.5 | 3.7 | 10.8 | 8.5 |
��1�����˹��õ���������Ҫ�ɷ���̼�ڣ�
��2����Һ�����������NaOH��Һ����pH��8.5〜8.8����Ŀ���dz�ȥFe3+��Zn2+��
��3�����ˢ�õ�����Һ�к��е���������Ҫ��Mn2+��NH4+��Na+�������ӷ��ţ���
��4�����̢��з�����Ӧ�����ӷ���ʽΪMn2++2HCO3-=MnCO3+CO2��+H2O��������A����ҺBӦ��ȡ�Ĵ��������ֱ���CO2ѭ�����ã���������NH4HCO3����ҺB�к���NH4Cl���ɷ����������ʣ�
��5�����̢ڵõ�MnO2����MnO2������Һ��ͨS02��ԭ�ɵ�MnSO4���ټ���Na2CO3��NaHCO3��Ҳ���Ʊ�MnCO3��SO2��ԭMnO2�Ļ�ѧ����ʽΪMnO2+S02=MnSO4����MnS04��Һ�м���Na2C03��NaHC03�Ʊ�MnC03ʱӦע��������DZ߽������Na2C03��NaHC03����������Һ��pH��8.8��
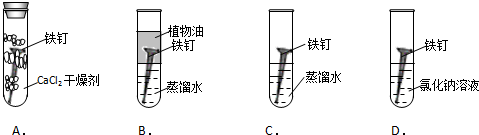
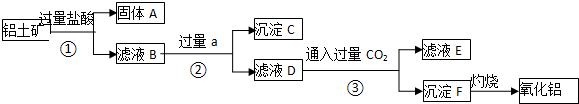
 ijѧ������ͼ��ʾװ�ý��л�ѧ��ӦX+2Y�T2Z�����仯������о��������Թ��еμ��Լ�Yʱ�����������м״�Һ���½����Ҵ�Һ�����������ڸ÷�Ӧ��������ȷ���ǣ�������
ijѧ������ͼ��ʾװ�ý��л�ѧ��ӦX+2Y�T2Z�����仯������о��������Թ��еμ��Լ�Yʱ�����������м״�Һ���½����Ҵ�Һ�����������ڸ÷�Ӧ��������ȷ���ǣ������� 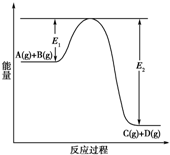 ��ӦA��g��+B��g��?C��g��+D��g�������е������仯����ͼ��ʾ���ش��������⣮
��ӦA��g��+B��g��?C��g��+D��g�������е������仯����ͼ��ʾ���ش��������⣮