题目内容
2. 如图是用高纯度固体二氧化钛生产金属钛的装置示意图,其原理是在较低的电压下,二氧化钛中的氧电离而进入熔融的氯化钙中,最后该电极只剩下纯净的金属钛.已知:熔融状态下,放电强弱为O2->Cl-.下列有关说法正确的是( )
如图是用高纯度固体二氧化钛生产金属钛的装置示意图,其原理是在较低的电压下,二氧化钛中的氧电离而进入熔融的氯化钙中,最后该电极只剩下纯净的金属钛.已知:熔融状态下,放电强弱为O2->Cl-.下列有关说法正确的是( )| A. | a电极为阴极 | |
| B. | a电极产生的气泡中主要成分是氯气 | |
| C. | 通电时,O2-、Cl-等向阴极移动 | |
| D. | 该制备工艺中需要定期更换石墨棒 |
分析 A、电解池的阳极是氧离子发生失电子的氧化反应;
B、根据电解池的阳极反应式去确定气泡主要成分;
C、电解池中,电解质里的阴离子移向阳极;
D、石墨电极会和阳极上产生的氧气之间发生反应.
解答 解:A、电解池的阳极是氧离子发生失电子的氧化反应,导致氧气等气体的出现,a电极为阳极,故A错误;
B、电解池的阳极是氧离子发生失电子的氧化反应,导致氧气等气体的出现电极反应式为:2O2-→O2↑+4e-,气泡中主要成分是氧气,故B错误;
C、电解池中,电解质里的阴离子O2-、Cl-均移向阳极,故C错误;
D、石墨电极会和阳极上产生的氧气之间发生反应,导致气体一氧化碳、二氧化碳的出现,所以电解本身会消耗,质量减轻,需要定期更换石墨棒,故D正确.
故选D.
点评 本题考查电解池的工作原理,题目难度不大,本题注意把握电极反应式的书写,图中电子的移动方向是解答的关键.

练习册系列答案
相关题目
18.化学是以实验为基础的自然科学,化学实验操作中必须十分重视安全问题和环境保护问题.下列实验问题处理方法正确的是( )
| A. | 浓硫酸不小心沾到皮肤上,立刻用NaOH溶液洗涤 | |
| B. | 实验结束后将所有的废液倒入下水道排出实验室,以免污染实验室 | |
| C. | 实验室制取气体时应先检查装置的气密性 | |
| D. | 做氢气还原氧化铜的实验时先加热再通氢气 |
16.下列有关实验原理或实验操作正确的是( )


| A. | 用广泛pH试纸测得饱和氯水的pH约为2.2 | |
| B. | 用量筒量取7.60 mL 0.1 mol•L-1盐酸 | |
| C. | 用图1所示的操作可检查装置的气密性 | |
| D. | 实验室用图2所示的装置制取少量的NO |
3.由FeO、Fe2O3、Fe3O4组成的混合物,测得其中铁元素与氧元素的质量比为21:8,则这种混合物中FeO、Fe2O3、Fe3O4的物质的量之比可能为( )
| A. | 1:2:1 | B. | 1:2:3 | C. | 1:3:1 | D. | 1:1:3 |
14.用如图实验装置和方法进行相应实验,能达到实验目的是( )
| A. | 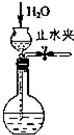 检查装置的气密性 | B. |  制取氨气 | ||
| C. |  进行石油分馏 | D. |  分离乙醇与乙酸 |
11.某固体NaOH因吸收了空气中的少量CO2而含有杂质,现在要将该固体NaOH配制成较纯的溶液,则其主要的实验操作过程应是( )
| A. | 溶解 加适量BaCl2溶液 过滤 | |
| B. | 溶解 加适量CaCl2溶液 过滤 | |
| C. | 溶解 加适量Ca(OH)2溶液 过滤 | |
| D. | 溶解 加适量盐酸 加热 |
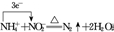 .
.